题目内容
【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
(提出问题)①氧化铜是否也能作氯酸钾分解的催化剂?是否比二氧化锰催化效果更好?
(设计并完成实验)
I、将 3.0g 氯酸钾放在试管中加热
II、将 3.0g 氯酸钾与 1.0g 二氧化锰均匀混合加热
III、将 Xg 氯酸钾与 1.0g 氧化铜均匀混合加热
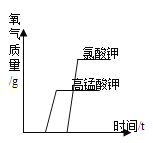
(实验现象分析)III 中 X 的值应为_____;将实验 I 和 III 比较可证明_____;
将实验反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到 1.0g 黑色粉末,再将黑色粉末和 Xg 氯酸钾混合加热, 现象与实验 III 相同,此步骤是为了证明氧化铜在该化学反应前后_____和_____都不变;
(结论)氧化铜也能作氯酸钾分解的催化剂。
(实验反思)实验 II 和 III 对比是为了证明_____;
(提出问题)②双氧水分解速度还和什么因素有关。
(设计并完成实验)
实验 | 双氧水的质量 | 双氧水的浓度 | MnO2 的质量 | 相同时间内产生 O2 体积 |
1 | 50.0g | 1% | 0.1g | 9mL |
2 | 50.0g | 2% | 0.1g | 16mL |
3 | 50.0g | 4% | 0.1g | 31mL |
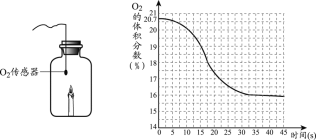
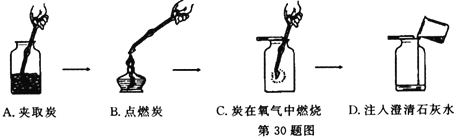
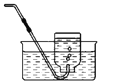
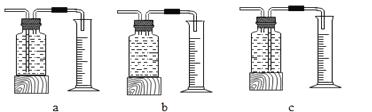
本实验中,测量 O2 体积的装置是_____(填编号)。
(结论)根据上表可知:在相同条件下,双氧水的浓度越大,双氧水分解的速率越_____。
【答案】3.0 氧化铜是否能作氯酸钾分解的催化剂 质量 化学性质 氧化铜是否比二氧化锰催化效果更好 C 快
【解析】
[实验现象分析]设计实验要注意控制变量,故III中X的值应为3.0,故填:3.0。
将实验I和III比较可证明氧化铜能加快氯酸钾的分解,故填:氧化铜能加快氯酸钾的分解;
将实验反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和Xg氯酸钾混合加热,现象与实验III相同,此步骤是为了证明氧化铜在该化学反应前后的质量和化学性质都不变,故填:质量;化学性质。
[结论]氧化铜还能作氯酸钾分解的催化剂,该化学反应的文字表达式为氯酸钾![]() 氯化钾+氧气
氯化钾+氧气
[实验反思]实验II和III中只有催化剂的类别不同,故对比是为了证明氧化铜和二氧化锰对氯酸钾分解速率的影响大小,故填:氧化铜和二氧化锰对氯酸钾分解速率的影响大小;
[设计并完成实验]
本实验中,氧气从短管进入才能将水从长管排出,故测量O2体积的装置是c,故填:c;
[结论]根据上表可知:在相同条件下,双氧水的浓度越大,双氧水分解得越快,故填:在相同条件下,双氧水的浓度越大,双氧水分解得越快。

 阅读快车系列答案
阅读快车系列答案【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是 ( )
实 验 装 置 |
硫在氧气中燃烧 |
排水法收集氧气 |
测定空气中氧气含量 |
铁丝在氧气中燃烧 |
解释 | 集气瓶中的水: 吸收放出的热量 | 集气瓶中的水: 水将集气瓶内的空气排干净,便于观察氧气何时收集满 | 量筒中的水: 通过水体积的变化得出氧气体积 | 集气瓶中的水: 冷却溅落熔化物,防止集气瓶炸裂 |
A | B | C | D |
A. A B. B C. C D. D
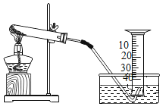
【题目】某兴趣小组对KClO3分解反应的催化剂进行研究,在相同的加热条件下,用如图装置完成表中实验:
编号 | KClO3质量/g | 催化剂 | 催化剂质量/g | 收集50mLO2所需时间/s |
实验1 | 5 | - | - | 171 |
实验2 | 5 | MnO2 | 0.5 | 49 |
实验3 | 5 | Fe2O3 | 0.5 | 58 |
实验4 | 5 | KCl | 0.5 | 154 |
(1)设置实验1的目的是___________________
(2)表中所列3种催化剂的催化效果最佳的是______________
(3)由实验1和实验4可知,KCl____(填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集收集50mLO2,所需时间明显少于171s,解释原因:______________。
(4)要比较KClO3分解反应中不同催化剂的催化效果,除了测量收集50mLO2所需时间外,还可以测量相同时间内________________。