题目内容
7.氮化硅是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定.工业上制备氮化硅的化学反应方程式为aSi+bN2$\frac{\underline{\;199℃\;}}{\;}$aSi3N4;则数值b=2,氮化硅属于盐.(填酸、碱、盐、氧化物)
分析 根据质量守恒定律:反应前后各原子的数目不变,进行分析解答.
酸是指在电离时产生的阳离子全部是氢离子的化合物;碱是指在电离时产生的阴离子全部是氢氧根离子的化合物;盐是由金属离子(或铵根离子)和酸根离子组成的化合物;氧化物是指由两种元素组成且一种是氧元素的化合物.
解答 解:由质量守恒定律,反应前后氮原子个数相等,则2b=4,b=2.
氮化硅是由硅离子和氮离子构成的化合物,属于盐.
故答案为:2;盐.
点评 本题难度不大,灵活运用质量守恒定律、酸碱盐与氧化物的特征是正确解答本题的关键.

练习册系列答案
相关题目
19.如表是部分物质的溶解性表(室温),利用表中提供的信息回答下列问题:
(1)NaOH和BaCl2两种物质混合后不能(填“能”或“不能”)发生反应,理由是交换成分没有沉淀、气体或水生成,不符合复分解反应发生的条件.
(2)利用表中阴离子和阳离子构成的物质,写出一个有BaSO4生成的化学方程式BaCl2+Na2SO4═BaSO4↓+2NaCl(合理即可).
| 阴离子 阳离子 | OH- | Cl- | SO42- |
| Na+ | 溶 | 溶 | 溶 |
| Fe2+ | 不 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 不 |
(2)利用表中阴离子和阳离子构成的物质,写出一个有BaSO4生成的化学方程式BaCl2+Na2SO4═BaSO4↓+2NaCl(合理即可).
2.下列不属于矿物燃料的是( )
| A. | 煤 | B. | 酒精 | C. | 天然气 | D. | 石油 |
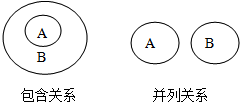 (1)物质分类概念存在如图所示的关系,单质与化合物属于并列关系(填“包含”或“并列”),化合物与氧化物属于包含关系(同上);
(1)物质分类概念存在如图所示的关系,单质与化合物属于并列关系(填“包含”或“并列”),化合物与氧化物属于包含关系(同上);
