题目内容
1.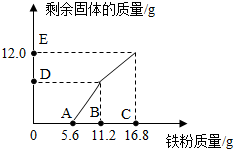 往FeCl3和CuCl2的混合溶液中逐渐加入铁粉.己知反应的先后顺序和化学方程式分别为:2FeCl3+Fe═3FeCl2 CuCl2+Fe═FeCl2+Cu.图为加入铁粉的质量与反应后剩余固体质量关系.则下列说法不正确的是( )
往FeCl3和CuCl2的混合溶液中逐渐加入铁粉.己知反应的先后顺序和化学方程式分别为:2FeCl3+Fe═3FeCl2 CuCl2+Fe═FeCl2+Cu.图为加入铁粉的质量与反应后剩余固体质量关系.则下列说法不正确的是( )| A. | D点对应纵坐标为6.4 | |
| B. | B点后溶液的颜色为蓝色 | |
| C. | AB两点间溶液的质量减小 | |
| D. | 取DE两点间的剩余固体加入盐酸,均有气泡产生 |
分析 分析图象可知:0-A段是铁与氯化铁反应,A-B段是铁与氯化铜反应,B-C段的质量=D-E段的质量,说明B-C段是铁粉剩余.
解答 解:A、B点处与氯化铜反应铁的质量为11.2g-5.6g=5.6g,设生成铜的质量为x,参加反应氯化铜的质量为y.
Fe+CuCl2═FeCl2+Cu
56 135 64
5.6g y x
则$\frac{56}{5.6g}=\frac{135}{y}=\frac{64}{x}$,x=6.4g,故此时生成铜为6.4g,也就是D点的坐标为6.4g,故A正确;
B、A点以前是铁与氯化铁反应,说明与氯化铁反应的铁为5.6g;A-B段是铁与氯化铜溶液反应,B点后溶液中无氯化铜,则不可能为蓝色,故B错误;
C、由图可知,AB两点固体质量增加,故AB两点间溶液的质量减小,故C正确;
D、由于由于DE两点间存在铁粉,所以加盐酸后一定能产生气泡,故D正确.
故选B.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
12.下列有关事实的结论合理的是( )
| 事实 | 结论 | |
| A | Al制品的耐腐蚀性比Cu制品强 | Al的活泼性弱于铜 |
| B | 金刚石和C60均是由碳元素组成的单质 | 金刚石和C60属于同一种物质 |
| C | 在“测定空气中氧气含量”的实验中,集气瓶内水面上升约$\frac{1}{5}$ | 氧气约占空气总质量的$\frac{1}{5}$ |
| D | H2O和CO2都不能使紫色石蕊变红,但把它们混合在一起时却能够使石蕊变红 | CO2与H2O发生了化学反应 |
| A. | A | B. | B | C. | C | D. | D |
9.在生产水泥的过程中,要大量优质的石灰石,某学校的课外兴趣小组的同学为了测定9765工厂的石灰石中碳酸钙的质量分数,取石灰石样品与足量的10%的稀盐酸在烧杯中反应,(杂质不反应也不溶于水)有关数据如表.
请计算(要写出过程):
(1)该石灰石样品中碳酸钙的质量分数;
(2)所消耗10%的稀盐酸的质量.
| 反 应 前 | 反 应 后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 133.4克 | 10克 | 140.1克 | |
(1)该石灰石样品中碳酸钙的质量分数;
(2)所消耗10%的稀盐酸的质量.
6.下列对某一主题的知识归纳,有错误的一组是( )
| A.化学常识 | B.化学与安全 |
| ?燃烧的条件--可燃物、氧气、温度达到着火点 ?硬水和软水--可用肥皂水来检验 | ?处理实验药品--将没有用完的白磷丢进垃圾筐 ?厨房煤气泄漏--立即打开排油烟机排出毒气 |
| C.化学与生活 | D.化学与能源 |
| ?青少年缺碘--易患甲状腺肿大 ?化纤织物、纯毛织物--用灼烧闻气味来鉴别 | ?沼气、酒精--生物能源,可再生能源 ?石 油、煤--化石能源,不可再生能源 |
| A. | A | B. | B | C. | C | D. | D |
11.实验室配制一定溶质质量分数的稀硫酸并用其除铁锈,部分操作如图所示,其中正确的是( )
| A. |  量取浓硫酸 | B. |  稀释浓硫酸 | C. |  装生锈铁钉 | D. |  倾倒稀硫酸 |
 请根据我们学过的化学知识填空.
请根据我们学过的化学知识填空.
 A~F是初中化学常见的6种物质,它们在一定条件下的转化关系如图所
A~F是初中化学常见的6种物质,它们在一定条件下的转化关系如图所 根据浙江省“五水共治”工作要求,舟山市提出“水安全、水生态、水景观、水文化、水经济”五位-体的治水新模式,目前针对高浓度有机废水的治理存在多元技术:
根据浙江省“五水共治”工作要求,舟山市提出“水安全、水生态、水景观、水文化、水经济”五位-体的治水新模式,目前针对高浓度有机废水的治理存在多元技术: