题目内容
9.在生产水泥的过程中,要大量优质的石灰石,某学校的课外兴趣小组的同学为了测定9765工厂的石灰石中碳酸钙的质量分数,取石灰石样品与足量的10%的稀盐酸在烧杯中反应,(杂质不反应也不溶于水)有关数据如表.| 反 应 前 | 反 应 后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 133.4克 | 10克 | 140.1克 | |
(1)该石灰石样品中碳酸钙的质量分数;
(2)所消耗10%的稀盐酸的质量.
分析 碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳;根据质量守恒定律,烧杯内质量的减少的质量即生成的二氧化碳质量,据此根据反应的化学方程式列式计算出参加反应碳酸钙的质量、盐酸的质量,进而计算出该石灰石中碳酸钙的质量分数、所消耗10%的盐酸的质量.
解答 解:由质量守恒定律,生成二氧化碳的质量为133.4g+10g-140.1g=3.3g.
设参加反应碳酸钙的质量为x,盐酸的质量的质量为y,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
x y 3.3g
$\frac{100}{x}=\frac{73}{y}=\frac{44}{3.3g}$
x=7.5g
y=5.475g
(1)此石灰石中碳酸钙的质量分数为:$\frac{7.5g}{10g}×$100%=75%.
(2)所消耗10%的稀盐酸的质量=$\frac{5.475g}{10%}$=54.75g
答案:
(1)此石灰石中碳酸钙的质量分数为75%;
(2)所消耗10%的稀盐酸的质量 54.75克.
点评 本题主要考查有关化学方程式的计算和质量分数的计算,难度较小.

练习册系列答案
相关题目
20.化学影响着社会的发展和人们的生活质量.以下分析不正确的是( )
| A. | 甲醛水溶液浸泡过的鱼,食用后不会危害人体健康 | |
| B. | 利用锂电池给数码相机供电 | |
| C. | 糖类和油脂都可以为人体提供能量 | |
| D. | 鸡蛋是富含蛋白质的食品 |
17.规范实验操作是获得实验成功的重要保证.下列实验操作正确的是( )
| A. |  闻气体气味 | B. |  取用块状固体 | C. |  滴加液体 | D. |  稀释浓硫酸 稀释浓硫酸 |
14.《舌尖上的中国》是中央电视台播出的美食类纪录片,2014年4月18日起播出第二季,主要内容为中国各地美食生态.厨房是制作美食的主要场地,下列在厨房发生的变化中,不属于化学变化的是( )
| A. |  苹果腐烂 | B. |  榨取果汁 | C. |  面包发霉 | D. |  菜刀生锈 |
1.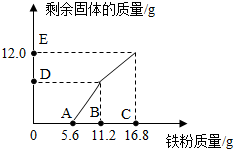 往FeCl3和CuCl2的混合溶液中逐渐加入铁粉.己知反应的先后顺序和化学方程式分别为:2FeCl3+Fe═3FeCl2 CuCl2+Fe═FeCl2+Cu.图为加入铁粉的质量与反应后剩余固体质量关系.则下列说法不正确的是( )
往FeCl3和CuCl2的混合溶液中逐渐加入铁粉.己知反应的先后顺序和化学方程式分别为:2FeCl3+Fe═3FeCl2 CuCl2+Fe═FeCl2+Cu.图为加入铁粉的质量与反应后剩余固体质量关系.则下列说法不正确的是( )
 往FeCl3和CuCl2的混合溶液中逐渐加入铁粉.己知反应的先后顺序和化学方程式分别为:2FeCl3+Fe═3FeCl2 CuCl2+Fe═FeCl2+Cu.图为加入铁粉的质量与反应后剩余固体质量关系.则下列说法不正确的是( )
往FeCl3和CuCl2的混合溶液中逐渐加入铁粉.己知反应的先后顺序和化学方程式分别为:2FeCl3+Fe═3FeCl2 CuCl2+Fe═FeCl2+Cu.图为加入铁粉的质量与反应后剩余固体质量关系.则下列说法不正确的是( )| A. | D点对应纵坐标为6.4 | |
| B. | B点后溶液的颜色为蓝色 | |
| C. | AB两点间溶液的质量减小 | |
| D. | 取DE两点间的剩余固体加入盐酸,均有气泡产生 |