题目内容
14.化学知识中有很多“相等”,下列有关说法中正确的是( )| A. | 化学反应前后,原子的种类和数目一定相等 | |
| B. | 饱和溶液析出晶体前后,其溶质质量分数一定相等 | |
| C. | 溶解度曲线相交,交点表示物质的溶质质量分数一定相等 | |
| D. | 将两种液体混合,混合后的体积与混合前两种液体体积之和一定相等 |
分析 A、根据质量守恒定律,进行分析判断.
B、根据饱和溶液析出晶体,可能是采用的降温结晶的方法,进行分析判断.
C、根据溶解度曲线相交,由交点的含义,进行分析判断.
D、根据分子间有间隔,进行分析判断.
解答 解:A、化学反应前后,遵守质量守恒定律,反应前后原子的种类和数目一定相等,故选项说法正确.
B、饱和溶液析出晶体,若采用的降温结晶的方法,溶质质量减少,溶剂质量不变,则溶质质量分数减小,故选项说法错误.
C、溶解度曲线相交,交点表示该温度下,两种物质的溶解度相等,但由于不知溶液是否饱和,物质的溶质质量分数不一定相等,故选项说法错误.
D、将两种液体混合,混合后的体积与混合前两种液体体积之和不相等,是因为分子之间有间隔,两种液体分子会互相占据分子之间的间隔,故选项说法错误.
故选:A.
点评 本题难度不大,掌握溶质质量分数的含义、溶解度曲线的含义、质量守恒定律等是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.已知R2O3的相对分子质量为160,则R的相对原子质量为( )
| A. | 32 | B. | 56 | C. | 27 | D. | 120 |
5.下列说法正确的是( )
| A. | 空气中二氧化碳含量的增加是形成酸雨的主要原因 | |
| B. | 利用乳化原理使用汽油洗去衣服上的油污 | |
| C. | 生活中可以用食醋去除水垢 | |
| D. | 聚乙烯塑枓属于天然有机高分子材料 |
19.氯酸钾的化学式为KClO3,在实验室常用于制取氧气,在氯酸钾中氯元素的化合价为( )
| A. | -1 | B. | +1 | C. | +3 | D. | +5 |
6.用下表中的仪器和药品组装一套实验装置,制取干燥的CO,用CO还原Fe2O3粉末,制得还原铁粉.制取CO的原理为:草酸H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$CO2↑+CO↑+H2O.
(1)上面连接的装置存在一明显的不足之处,请在表格的E空白处画图说明.
(2)如果所制气体流向从左向右时,上述组装的实验装置从左向右连接顺序是ADBCE(填序号).
(3)在连接好装置后操作第一步应是连接好装置并检查气密性;最后一步应是熄灭E处的酒精灯.
| 序号 | A | B | C | D | E |
| 仪器 药品 |  |  浓硫酸 |  |  NaOH溶液 |
(2)如果所制气体流向从左向右时,上述组装的实验装置从左向右连接顺序是ADBCE(填序号).
(3)在连接好装置后操作第一步应是连接好装置并检查气密性;最后一步应是熄灭E处的酒精灯.
4.如表是氯化钾和硝酸钾在不同温度时的溶解度.图1是这两种物质的溶解度曲线,图2是相同质量的这两种物质在某温度时分别溶于相同质量的水中的情况.

(1)图1中,t1℃时,b的饱和溶液中溶质与溶液的质量比为1:3.
(2)图2中③、④分别是①、②升温后的情况,则图2中肯定属于饱和溶液的是②(填序号);溶质质量分数变大的是硝酸钾(填物质名称).
(3)图1中t1的温度范围是30℃<t1<40℃.
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | |
| 溶解度(g) | KCl | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 |
| KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |

(1)图1中,t1℃时,b的饱和溶液中溶质与溶液的质量比为1:3.
(2)图2中③、④分别是①、②升温后的情况,则图2中肯定属于饱和溶液的是②(填序号);溶质质量分数变大的是硝酸钾(填物质名称).
(3)图1中t1的温度范围是30℃<t1<40℃.
 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答: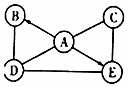 A、B、C、D、E是初中化学常见的五种不同类别的物质.其中B的固体可用于人工降雨,C的组成元素在地壳中含量居第四位,D常用于清洗油污.图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略).请回答下列问题.
A、B、C、D、E是初中化学常见的五种不同类别的物质.其中B的固体可用于人工降雨,C的组成元素在地壳中含量居第四位,D常用于清洗油污.图中“-”表示相连物质能发生化学反应,“→”表示两种物质间的转化关系(部分反应物、生成物及反应条件省略).请回答下列问题.