题目内容
15.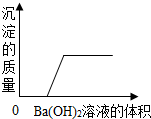 某溶液由盐酸、碳酸钠溶液、稀硫酸、氯化铜溶液四种物质中的一种或几种混合形成,现向该混合溶液中滴入氢氧化钡溶液,产生沉淀的质量与加入氢氧化钡溶液体积的关系如图所示.
某溶液由盐酸、碳酸钠溶液、稀硫酸、氯化铜溶液四种物质中的一种或几种混合形成,现向该混合溶液中滴入氢氧化钡溶液,产生沉淀的质量与加入氢氧化钡溶液体积的关系如图所示.(1)请写出溶液中的溶质的化学式HCl;CuCl2
(2)写出产生沉淀时所发生的化学反应方程式Ba(OH)2+CuCl2=BaCl2+Cu(OH)2↓.
分析 根据钡离子一接触硫酸根离子就会生成沉淀,铜离子和氢氧根离子会生成氢氧化铜沉淀,加入一定体积后才出现沉淀,说明开始是在发生中和反应,所以一定存在盐酸,盐酸和碳酸钠不能共存,就不存在碳酸钠进行分析.
解答 解:氢氧化钡只要遇到硫酸就会生成沉淀,而图象是一段体积后,才开始出现沉淀,说明了一定没有硫酸,开始加入的氢氧化钡发生的是中和反应,说明存在盐酸,盐酸和碳酸钠反应,就不存在碳酸钠,还得会和氢氧化钡生成沉淀,一定存在氯化铜.
(1)溶液中的溶质是氯化氢和氯化铜,化学式分别为:HCl;CuCl2;
(2)氯化铜和氢氧化钡反应生成氯化钡和氢氧化铜沉淀,反应的化学方程式为:Ba(OH)2+CuCl2=BaCl2+Cu(OH)2↓;
答案:
(1)HCl;CuCl2;
(2)Ba(OH)2+CuCl2=BaCl2+Cu(OH)2↓;
点评 在解此类题时,要学会认知图象,根据图象中的数据进行分析存在的物质和不存在的物质,然后结合推出的物质再验证其他的物质.

练习册系列答案
相关题目
6.“低钠盐”可以控制钠的摄入量从而防治高血压等疾病.制备“低钠盐”是在食盐中用NaCl按照配方比例添加食用KCl.国内某些生产厂家为改变“低钠盐”口味还会加入少量镁盐(仅限MgSO4或MgCl2).
(1)测得某“低钠盐”样品a中只含有NaCl和KCl,该样品中的NaCl和KCl溶于水时解离出的阴离子都是Cl-(填离子符号).
(2)探究某“低钠盐”样品b中是否添加有镁盐,以及添加的是何种镁盐?
【猜想】I、不含镁盐Ⅱ、含有硫酸镁Ⅲ、含有氯化镁
【进行实验】

(3)请完成如表(已知BaSO4是难溶于水和酸的白色固体):
(1)测得某“低钠盐”样品a中只含有NaCl和KCl,该样品中的NaCl和KCl溶于水时解离出的阴离子都是Cl-(填离子符号).
(2)探究某“低钠盐”样品b中是否添加有镁盐,以及添加的是何种镁盐?
【猜想】I、不含镁盐Ⅱ、含有硫酸镁Ⅲ、含有氯化镁
【进行实验】

(3)请完成如表(已知BaSO4是难溶于水和酸的白色固体):
| 假设和现象 | 判断和化学方程式 | |
| ① | 若现象a为白色沉淀 | 则猜想I不成立. |
| ② | 若现象a为产生白色沉淀, 现象b为无明显现象. | 则猜想Ⅲ成立.写出无色溶液B与硝酸中和反 应的化学方程式NaOH+HNO3=NaNO3+H2O. |
| ③ | 若现象a、b均 为:产生白色沉淀 | 则猜想Ⅱ成立.写出无色溶液B与硝酸钡溶液 反应的化学方程式Ba(NO3)2+Na2SO4=BaSO4↓+2NaNO3. |
20.下列图象分别与选项中的操作相对应,其中合理的是( )
| A. | 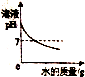 向一定量稀氢氧化钠溶液中滴入水 | |
| B. |  向一定量氯化铜溶液中加入一定量铝 | |
| C. |  向一定量硫酸和硫酸铜混合溶液中滴入氢氧化钠溶液 | |
| D. |  等质量的稀硫酸分别与足量的镁、铁、锌三种金属反应 |
4.生活处处有化学,下列说法不正确的是( )
| A. | 钛具有极强的抗腐蚀性,可制造轮船外壳 | |
| B. | 用汽油去除油污原因是汽油对油污有乳化作用 | |
| C. | 铝和空气中的氧气反应生成致密的氧化铝薄膜,所以铝制品抗腐浊性强 | |
| D. | 在南方沿海地区的铁制品比北方更容易生锈是因为南方空气湿度大、温度高 |
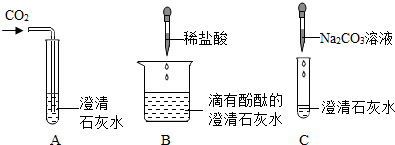



 如图是A、B、C三种物质的溶解度随温度变化的曲线图.
如图是A、B、C三种物质的溶解度随温度变化的曲线图.