题目内容
实验室制取1mol O2,需H2O2________克.等物质量的H2O2和H2O中原子总数之比为________.电解1mol H2O所得O2的量和分解________mol H2O2所得的O2量相当.
68 4:3 1
分析:根据H2O2制取氧气的化学方程式,由氧气的物质的量计算需H2O2的质量;根据化学式的意义计算等物质量的H2O2和H2O中原子总数之比;根据电解水及分解双氧水制取氧气的方程式,分析判定得到相同氧气的物质的量时,水和双氧水的物质的量的关系.
解答:设实验室制取1mol O2需要H2O2的物质的量为x,则
2H2O2 2H2O+O2↑
2H2O+O2↑
2 1
x 1mol
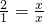 x=2mol
x=2mol
2molH2O2的质量为:2mol×34g/mol=68g
由化学式的意义可知:等物质量的H2O2和H2O中原子总数之比为4:3;
由化学方程式:2H2O2 2H2O+O2↑,2H2O
2H2O+O2↑,2H2O 2H2↑+O2↑
2H2↑+O2↑
可知制取相同物质的量的氧气,需双氧水和电解水的物质的量的关系是:2H2O2~2H2O~O2
所以电解1molH2O所得O2的量和分解1molH2O2所得的O2量相当.
故答为:68,4:3,1
点评:本题主要考查了根据化学方程式的计算,会根据化学方程式进行有关物质的计算.
分析:根据H2O2制取氧气的化学方程式,由氧气的物质的量计算需H2O2的质量;根据化学式的意义计算等物质量的H2O2和H2O中原子总数之比;根据电解水及分解双氧水制取氧气的方程式,分析判定得到相同氧气的物质的量时,水和双氧水的物质的量的关系.
解答:设实验室制取1mol O2需要H2O2的物质的量为x,则
2H2O2
 2H2O+O2↑
2H2O+O2↑2 1
x 1mol
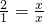 x=2mol
x=2mol2molH2O2的质量为:2mol×34g/mol=68g
由化学式的意义可知:等物质量的H2O2和H2O中原子总数之比为4:3;
由化学方程式:2H2O2
 2H2O+O2↑,2H2O
2H2O+O2↑,2H2O 2H2↑+O2↑
2H2↑+O2↑可知制取相同物质的量的氧气,需双氧水和电解水的物质的量的关系是:2H2O2~2H2O~O2
所以电解1molH2O所得O2的量和分解1molH2O2所得的O2量相当.
故答为:68,4:3,1
点评:本题主要考查了根据化学方程式的计算,会根据化学方程式进行有关物质的计算.

练习册系列答案
相关题目
下图甲~己是实验室制取某些常见气体的装置图.
(1)仪器a、b的名称是a 、b ;
(2)甲装置可用于实验室制取O2,写出该反应的化学方程式 ;
(3)以下方案是对排水法与排空气法收集O2的比较(使用体积相同的集气瓶收集O2)
(4)装置乙和丙都能用于实验室制取CO2,丙相对于乙在操作方面的优点为 ;
(5)使用丁装置制取气体时,对反应物和反应条件的要求是 ;
(6)用块状的石灰石与过量稀盐酸反应制取CO2,若参加反应的碳酸钙的物质的量为0.1mol,请回答:
Ⅰ.反应生成CO2的物质的量为 (根据化学方程式列式计算);
Ⅱ.待块状石灰石与过量稀盐酸反应至不再冒气泡后,过滤反应后的混合物,并向滤液中逐滴滴入碳酸钠溶液,并用pH数字探测仪连续监测,得到如下曲线:

(已知CaCl2溶液呈中性)
①写出AB段反应的实验现象 ;
②BC段的反应生成了白色沉淀,写出该反应的化学方程式 ;
③DE段所对应溶液中的溶质有NaCl和 .

(1)仪器a、b的名称是a
(2)甲装置可用于实验室制取O2,写出该反应的化学方程式
(3)以下方案是对排水法与排空气法收集O2的比较(使用体积相同的集气瓶收集O2)
| 比较项目 | 向上排空气法 | 排水集气法 | 结论 |
| 方法可行性 | O2的密度比空气 |
O2难溶于水且不与水反应 | 两种方法均可行 |
| 收集的过程 | “验满”分析:即便用带火星的木条移近集气瓶口,木条复燃也难以证明空气被排尽,因气体无色,集满与否较难确定. | 集满O2的现象是 |
排水法收集O2更易于观察何时集满 |
| 收集O2的纯度 | 分别用排水法和向上排空气法收集两瓶氧气(A和B),放入两支相同的蜡烛.可观察到B瓶内的蜡烛熄灭较早 |
结论 | |
(5)使用丁装置制取气体时,对反应物和反应条件的要求是
(6)用块状的石灰石与过量稀盐酸反应制取CO2,若参加反应的碳酸钙的物质的量为0.1mol,请回答:
Ⅰ.反应生成CO2的物质的量为
Ⅱ.待块状石灰石与过量稀盐酸反应至不再冒气泡后,过滤反应后的混合物,并向滤液中逐滴滴入碳酸钠溶液,并用pH数字探测仪连续监测,得到如下曲线:

(已知CaCl2溶液呈中性)
①写出AB段反应的实验现象
②BC段的反应生成了白色沉淀,写出该反应的化学方程式
③DE段所对应溶液中的溶质有NaCl和
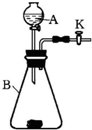 在学习了实验室制取CO2之后,联想到该装置也用于在实验室中用H2O2制取氧气.
在学习了实验室制取CO2之后,联想到该装置也用于在实验室中用H2O2制取氧气.