题目内容
10.某食盐样品中含有少量CaCl2,根据图示信息计算该食盐样品中NaCl的质量分数.
分析 由于氯化钠和氯化钙中只有氯化钙和碳酸钠反应生成沉淀,题目给出了沉淀碳酸钙的质量,根据碳酸钙的质量和对应的化学方程式可以求算氯化钙的质量,进而求得原混合物中氯化钠的质量分数.
解答 解:设样品中氯化钙的质量为x
CaCl2+Na2CO3=CaCO3↓+2NaCl
111 100
x 2.0g
$\frac{111}{100}$=$\frac{x}{2.0g}$
x=2.22g
样品中氯化钠的质量分数为$\frac{10g-2.22g}{10g}$×100%=77.8%
答:样品中氯化钠的质量分数为77.8%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
相关题目
20.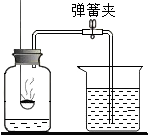 如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中不正确的是( )
如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中不正确的是( )
 如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中不正确的是( )
如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列说法中不正确的是( )| A. | 该实验证明空气中氧气的含量约占$\frac{1}{5}$ | |
| B. | 实验时红磷一定要过量 | |
| C. | 实验前一定要检验装置的气密性 | |
| D. | 红磷燃烧产生大量的白烟,火焰熄灭后立刻打开弹簧夹 |
18.下列关于干冰灭火的说法不正确的是( )
| A. | 干冰升华时吸热,能降低可燃物的着火点 | |
| B. | CO2覆在可燃物表面,隔绝空气 | |
| C. | CO2不能支持燃烧 | |
| D. | 干冰升华后不污染档案资料 |
2.世博“零碳馆”是中国第一座“零碳”排放的公共建筑,这里“碳”是指( )
| A. | 碳酸 | B. | 一氧化碳 | C. | 炭黑 | D. | 二氧化碳 |
20.小明同学在家中带来了一个废弃的水龙头,其成分为黄铜(铜锌合金),为了测定黄铜中铜的质量分数,在老师的指导下做了如下实验,有关实验数据记录如表:
请分析实验数据,完成下列计算
(1)第2次实验中a的数值为111.8.
(2)该黄铜样品中铜的质量分数?(请写出计算过程,计算结果精确到0.1%)
(3)第4此实验中,充分反应后溶液中溶质的成分为H2SO4、ZnSO4(写化学式).
| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 所取黄铜样品的质量(g) | 32.0 | 32.0 | 32.0 | 32.0 |
| 加入稀硫酸的质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 反应后烧杯内剩余物质的质量(g) | 71.9 | a | 151.7 | 191.7 |
(1)第2次实验中a的数值为111.8.
(2)该黄铜样品中铜的质量分数?(请写出计算过程,计算结果精确到0.1%)
(3)第4此实验中,充分反应后溶液中溶质的成分为H2SO4、ZnSO4(写化学式).
 如图为硫酸镁的溶解度曲线,请回答:
如图为硫酸镁的溶解度曲线,请回答: