题目内容
 实验室新进一批块状大理石.某化学兴趣小组成员称取烧杯和大理石样品共132.5g,加入足量100克稀盐酸完全反应后,称得烧杯及剩余物的质量为228.1g.样品中杂质不溶于水且不与稀盐酸反应,请回答下列问题:
实验室新进一批块状大理石.某化学兴趣小组成员称取烧杯和大理石样品共132.5g,加入足量100克稀盐酸完全反应后,称得烧杯及剩余物的质量为228.1g.样品中杂质不溶于水且不与稀盐酸反应,请回答下列问题:(1)计算该样品中碳酸钙的质量.
(2)若要求出该大理石样品中含碳酸钙的质量分数,还需要知道什么数据
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据质量守恒定律需先求出二氧化碳的质量,在根据化学方程式中的质量比进而求出碳酸钙的质量;
(2)若要求出该大理石样品中含碳酸钙的质量分数,还需要知道烧杯的质量才能计算出碳酸钙样品的质量;
(2)若要求出该大理石样品中含碳酸钙的质量分数,还需要知道烧杯的质量才能计算出碳酸钙样品的质量;
解答:解:(1)生成CO2的质量为 132.5g+100g-228.1g=4.4g
设样品中的碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
=
x=10g
(2)若要求出该大理石样品中含碳酸钙的质量分数,还需要知道烧杯的质量才能计算出碳酸钙样品的质量;
答案:(1)10g;
(2)烧杯的质量
设样品中的碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
| 100 |
| x |
| 44 |
| 4.4g |
x=10g
(2)若要求出该大理石样品中含碳酸钙的质量分数,还需要知道烧杯的质量才能计算出碳酸钙样品的质量;
答案:(1)10g;
(2)烧杯的质量
点评:本题难度不是很大,主要考查了学生分析题意获取选项及根据化学方程式进行有关的计算,培养学生分析问题的能力和解决问题的能力.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案
相关题目

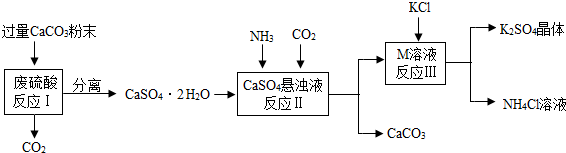

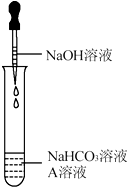 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.