题目内容
18.在含有 FeCl3、FeCl2、AlCl3、NaCl的溶液中,加入足量的NaOH溶液,在空气中充分搅拌,反应后再加入过量的稀盐酸,溶液中离子数目减少的是( )| A. | Na+ | B. | Fe3+ | C. | Al3+ | D. | Fe2+ |
分析 加入氢氧化钠,溶液中钠离子增多,氢氧化钠与FeCl3、FeCl2、AlCl3反应,产物再与空气中的氧气以及过量的盐酸反应,据此分析.
解答 解:向溶液中加入NaOH,溶液中钠离子增多,故A错误;
氢氧化钠分别与FeCl3、FeCl2、AlCl3反应的方程式为:
FeCl3+3NaOH═Fe(OH)3↓+3NaCl,
FeCl2+2NaOH=Fe(OH)2↓+2NaCl,
AlCl3(过量)+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3+NaOH═NaAlO2+2H2O,
从方程式看出分别生成氢氧化铁沉淀、氢氧化亚铁沉淀、偏铝酸钠,而偏铝酸钠与过量的盐酸反应生成铝离子,铝离子数目没有变化.故C错误;
生成氢氧化亚铁与空气中氧气反应全部生成氢氧化铁反应为4Fe(OH)2+2H2O+O2═4Fe(OH)3.然后再加入过量的盐酸,氢氧化铁与盐酸反应生成氯化铁,三价铁离子数目增多,二价铁离子减少.故B错误,D正确;
故选D.
点评 本题主要考查了二价铁离子和三价铁离子间的相互转化,解题时需灵活运用有关化学反应方程式.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
9.化学知识就在我们身边,以下叙述中发生化学变化的是( )
| A. | 水放进冰箱一段时间后结成冰 | B. | 不小心玻璃容器被摔碎 | ||
| C. | 剩余的食物放一段时间后变质 | D. | 湿衣服经太阳晒后很快变干 |
6.用铝箔包裹着2.3g金属钠投入到足量水中,理论上可以收集到氢气的物质的量为( )
| A. | 0.05mol | B. | 0.2mol | ||
| C. | 大于0.05mol小于或等于0.2mol | D. | 无法判断 |
13.下列物质不能通过化合反应生成的是( )
| A. | NaOH | B. | NaHCO3 | C. | FeCl2 | D. | Al(OH)3 |
3.推理是一种重要的学习和研究方法.下列推理正确的是( )
| A. | 单质中只含一种元素,所以只含一种元素的物质一定是单质 | |
| B. | 化学变化前后物质的质量总和不变,所以1gH2和1gO2一定能够生成2gH2O | |
| C. | 碱性溶液能使酚酞溶液变红,所以能使酚酞溶液变红的物质一定呈碱性 | |
| D. | 中和反应有盐和水生成,所以有盐和水生的反应一定是中和反应 |
7.将一定量的双氧水和3克的二氧化锰混合,充分反应,测得反应的总质量(m)与反应肘间(t)的数据如下表所示:
根据题目要求,问双氧水的物质的量是多少?(通过化学方程式列式计算)
| 反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 |
| 总质量m/g | 50 | 49.0 | 48.1 | 47.3 | 46.8 | 46.8 |
8.在10%的氯化钠溶液中,溶质、溶剂、溶液之间的质量关系正确的是( )
| A. | 溶质:溶剂=1:10 | B. | 溶质:溶液=1:9 | C. | 溶剂:溶液=9:10 | D. | 溶质:溶液=1:11 |

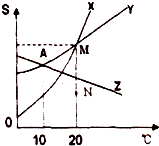 图是X、Y、Z三种物质的溶解度曲线,
图是X、Y、Z三种物质的溶解度曲线,