题目内容
20℃时氯化钠的溶解度为36g,20℃时,将20g氯化钠放入50g水中充分溶解,所得溶液中溶质的质量分数为( )
| A、20% | B、26.5% |
| C、36% | D、4O% |
考点:有关溶质质量分数的简单计算
专题:溶液的组成及溶质质量分数的计算
分析:溶解度是在一定温度下,某固体溶质在100g溶剂里达到饱和状态所溶解的溶质质量,判断50克水溶解的氯化钠的质量,据此由溶质的质量分数=溶质质量分数=
×100%,进行分析解答.
| 溶质质量 |
| 溶液质量 |
解答:解:根据溶解度的概念,20℃时氯化钠的溶解度是36g,其涵义是20℃时,100g水中最多溶解36g氯化钠,溶液达到饱和状态.20℃时,将20g氯化钠放入50g水中充分溶解,最多只能溶解18g,所得溶液中溶质的质量分数为
×100%≈26.5%.
故选:B.
| 18g |
| 18g+50g |
故选:B.
点评:本题难度不大,掌握溶解度的含义、溶质质量分数的有关计算并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
下列关于水的叙述,错误的是( )
| A、生活中通过煮沸可降低水的硬度 |
| B、生活污水直接排放不会造成水污染 |
| C、水是由水分子构成的 |
| D、净化水的方法有吸附、沉淀、过滤和蒸馏 |
如图所示实验操作,不正确的是( )
A、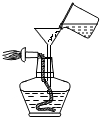 添加酒精 |
B、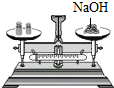 称量氢氧化钠 |
C、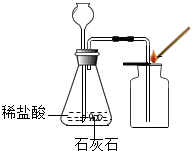 制取二氧化碳并验满 |
D、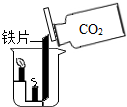 二氧化碳性质检验 二氧化碳性质检验 |
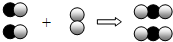 如图是用来表示物质间发生化学变化的模型示意图,图中“
如图是用来表示物质间发生化学变化的模型示意图,图中“
 ”分别表示两种不同元素的原子.依据下列信息,有关说法错误的是( )
”分别表示两种不同元素的原子.依据下列信息,有关说法错误的是( )| A、反应前后分子的种类发生了改变 |
| B、反应前后没有元素化合价的改变 |
| C、该反应符合质量守恒定律 |
| D、该反应属于化合反应 |
只用一种试剂,一次性验证铜、铁、银三种金属的活动性强弱,该试剂是( )
| A、CuSO4溶液 |
| B、AgNO3溶液 |
| C、FeSO4溶液 |
| D、稀硫酸 |
下列实验现象的描述中,不正确的是( )
| A、木炭在氧气中燃烧发出白光 |
| B、细铁丝在氧气中燃烧火星四射 |
| C、蜡烛在氧气中燃烧发出白光,瓶壁上出现液滴 |
| D、硫在氧气中燃烧发出淡蓝色火焰 |
下列做法不会造成环境污染的是( )
| A、燃放烟花爆竹 |
| B、汽车排放的废气 |
| C、利用太阳能发电 |
| D、拆房修路 |
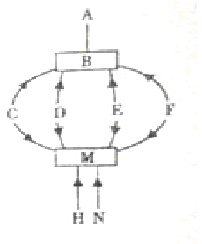 右图为九种物质的相互关系,其中A、B、M、N是氧化物,C、H是单质,只有D、E中含有三种元素,D能使紫色石蕊溶液变成红色.图中“→”化
右图为九种物质的相互关系,其中A、B、M、N是氧化物,C、H是单质,只有D、E中含有三种元素,D能使紫色石蕊溶液变成红色.图中“→”化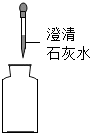


 冷水
冷水