题目内容
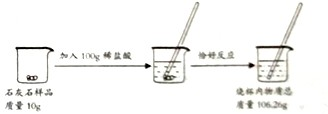
某兴趣小组要测定某石灰石样品中杂质的质量分数,他们进行了如图实验,(杂质不发生反应)请计算:
(1)生成CO2气体的质量;
(2)样品中杂质的质量分数;
(1)生成CO2气体的质量;
(2)样品中杂质的质量分数;

考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据质量守恒定律可知:反应后比反应前减少的质量是生成二氧化碳的质量;
(2)根据化学方程式由二氧化碳的质量可以计算出石灰石中碳酸钙的质量,进而计算出石灰石中杂质的质量分数.
(2)根据化学方程式由二氧化碳的质量可以计算出石灰石中碳酸钙的质量,进而计算出石灰石中杂质的质量分数.
解答:解:解:(1)根据质量守恒定律,二氧化碳的质量为:10g+100g-106.2g=3.8g.
(2)设该石灰石样品中碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 3.8g
=
解得:x≈8.64g
(2)样品中杂质的质量分数为:
×100%=13.6%
答:(1)生成CO2气体的质量为3.8g;
(2)样品中杂质的质量分数为13.6%.
(2)设该石灰石样品中碳酸钙的质量为x.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 3.8g
| 100 |
| x |
| 44 |
| 3.8g |
解得:x≈8.64g
(2)样品中杂质的质量分数为:
| 10g-8.64g |
| 10g |
答:(1)生成CO2气体的质量为3.8g;
(2)样品中杂质的质量分数为13.6%.
点评:本题主要考查学生运用所学化学知识分析和解决实际问题的能力,增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列图示的实验操作中,正确的是( )
A、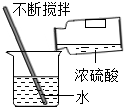 稀释浓硫酸 |
B、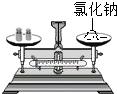 称取氯化钠 |
C、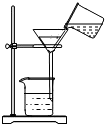 过滤 |
D、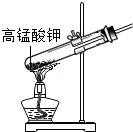 制取氧气 |