题目内容
12.已知硫的核电荷数为16,对于S和S2-的说法,正确的是( )| A. | 属于同一种元素 | B. | 化学性质相同 | ||
| C. | 核外电子数相同 | D. | 具有不同的电子层数 |
分析 硫原子得到2个电子形成硫离子;根据同种元素的质子数相同,原子中质子数等于其核电荷数,原子的质量主要集中在原子核上等,据此分析判断即可.
解答 解:A、硫原子得到2个电子形成硫离子,S和S2-的质子数相同,它们属于同种元素,故正确.
B、元素的化学性质取决于微粒的最外层电子数,两者最外层电子数不同所以化学性质不同;故错误;
C、硫原子得到2个电子形成硫离子,它们的核外电子数不同,故错误.
D、硫原子得到两个电子形成硫离子时电子层数没变,故电子层数相同,故错误.
故选:A.
点评 本题难度不大,掌握原子和离子的相互转化、元素的特征、原子的构成等并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
2.如果一个碳-12原子的相对原子质量为24,则不会改变的是( )
| A. | 相对原子质量计算公式中的标准 | B. | 氧原子的相对原子质量 | ||
| C. | 硫酸的相对分子质量 | D. | 一个碳-12原子的质量 |
20.请应用质量守恒定律的有关知识,完成下列各题.
(1)硅(Si )是太阳能电池和电脑芯片中不可缺少的材料.生产硅的化学反应为SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2X↑.则X 的化学式为CO.
(2)过氧化钙(CaO2)常用于鱼池供氧剂,它与水反应,生成氧气和氢氧化钙,该反应的化学方程式为2CaO2+2H2O=2Ca(OH)2+O2↑.
(3)在一密闭容器内有氧气、二氧化碳、水蒸气和一种未知物W,在一定条件下充分反应,测得反应前后各物质的质量如下表所示.
①X的数值为0.
反应物是W、氧气. 分别反应了23、48克
生成物是二氧化碳、水. 分别生成了44、27克
②W中含有的元素是C、O、H.分别为12、3、8克
③W的化学式为C2H6O
(4)如图是工业上制备氢气的微观示意图,其中不同的“球”代表不同的原子.下列说法不正确的是AC(填字母序号).
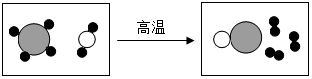
A.反应前后,分子个数不变
B.反应前后,原子的种类、数目不变
C.该反应中共涉及两种单质和三种化合物
D.该反应中参加反应的两种分子的个数比为1:1.
(1)硅(Si )是太阳能电池和电脑芯片中不可缺少的材料.生产硅的化学反应为SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2X↑.则X 的化学式为CO.
(2)过氧化钙(CaO2)常用于鱼池供氧剂,它与水反应,生成氧气和氢氧化钙,该反应的化学方程式为2CaO2+2H2O=2Ca(OH)2+O2↑.
(3)在一密闭容器内有氧气、二氧化碳、水蒸气和一种未知物W,在一定条件下充分反应,测得反应前后各物质的质量如下表所示.
| 物 质 | 氧 气 | 二氧化碳 | 水蒸气 | W |
| 反应前质量/g | 50 | 1 | 1 | 23 |
| 反应后质量/g | 2 | 45 | 28 | x |
反应物是W、氧气. 分别反应了23、48克
生成物是二氧化碳、水. 分别生成了44、27克
②W中含有的元素是C、O、H.分别为12、3、8克
③W的化学式为C2H6O
(4)如图是工业上制备氢气的微观示意图,其中不同的“球”代表不同的原子.下列说法不正确的是AC(填字母序号).

A.反应前后,分子个数不变
B.反应前后,原子的种类、数目不变
C.该反应中共涉及两种单质和三种化合物
D.该反应中参加反应的两种分子的个数比为1:1.
17.一定质量的某化合物完全燃烧,消耗9.6g氧气,生成8.8g二氧化碳和5.4g水.对该化合物的组成判断正确的是( )
| A. | 只含有C、H两种元素 | B. | 含有C、H、O三种元素 | ||
| C. | 分子中C、H原子个数比为3:1 | D. | 以上答案都不正确 |
1.前者属于物理变化,后者属于化学变化的是( )
| A. | 水结成冰,冰融化成水 | B. | 鸡蛋变臭,人体呼吸 | ||
| C. | 酒精挥发,酒精燃烧 | D. | 铁生锈,电灯通电发光 |
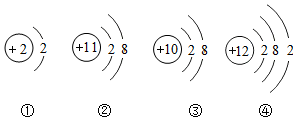 根据下列几种粒子的结构示意图,回答问题.
根据下列几种粒子的结构示意图,回答问题.