题目内容
8.某化学兴趣小组同学取ag氯酸钾和2g二氧化锰加热制取氧气并进行如下操作.
(1)滴加硝酸银溶液时发生反应的化学方程式为KCl+AgNO3═AgCl↓+KNO3.
(2)固体M的成分KCl、MnO2(填化学式);
(3)M中与硝酸银反应的物质的质量为X,列出求解x的比例式$\frac{74.5}{x}$=$\frac{143.5}{14.35g}$;
(4)加入的氯酸钾质量为12.25g.
(5)加入硝酸银溶液质量分数为10%.
分析 氯酸钾在二氧化锰的催化作用下受热分解生成氯化钾和氧气;
氯化钾和硝酸银反应生成白色沉淀氯化银和硝酸钾,根据提供的数据可以进行相关方面的计算.
解答 解:(1)滴加硝酸银溶液时,硝酸银和氯化钾反应生成氯化银和硝酸钾,发生反应的化学方程式为:KCl+AgNO3═AgCl↓+KNO3.
故填:KCl+AgNO3═AgCl↓+KNO3.
(2)固体M中含有氯化钾和二氧化锰,化学式是KCl、MnO2.
故填:KCl、MnO2.
(3)设硝酸银的质量为m,生成硝酸钾的质量为n,
M中与硝酸银反应的物质是氯化钾,滤渣质量是16.35g,则氯化银的质量为:16.35g-2g=14.35g,
KCl+AgNO3═AgCl↓+KNO3,
74.5 170 143.5 101
x m 14.35g n
$\frac{74.5}{x}$=$\frac{170}{m}$=$\frac{143.5}{14.35g}$=$\frac{101}{n}$,
x=7.45g,m=17g,n=10.1g,
故填:$\frac{74.5}{x}$=$\frac{143.5}{14.35g}$.
(4)设氯酸钾的质量为y,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,
245 149
y 7.45g
$\frac{245}{y}$=$\frac{149}{7.45g}$,
y=12.25g,
故填:12.25g.
(5)根据题意有:(7.45g+38.9g+bg-14.35g-151.5g)×20%=10.1g,
b=170,
则加入硝酸银溶液质量分数为:$\frac{17g}{170g}$×100%=10%,
故填:10%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

 阅读快车系列答案
阅读快车系列答案| A. | 液氢可用作制冷剂 | |
| B. | 氧气可用作火箭发射的燃料 | |
| C. | 氦气也用作填充探空气球 | |
| D. | 二氧化碳是植物进行光合作用必须的物质 |
| A. | 酒精挥发------分子是运动的 | |
| B. | 夏天钢轨之间的缝隙变小------分子之间有间隔 | |
| C. | 糖是甜的,醋是酸的-----不同分子性质不同 | |
| D. | 电解水制取氢气和氧气-----分子在化学反应中可以再分 |
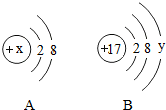 如图中A、B分别是某粒子的结构示意图,回答下列问题
如图中A、B分别是某粒子的结构示意图,回答下列问题
 ”表示氢原子,用“
”表示氢原子,用“ ”表示氧原子,用“
”表示氧原子,用“ ”表示硫原子,上述反应过程可用如图2表示,该反应的化学方程式为2H2S+SO2=3S+2H2O;
”表示硫原子,上述反应过程可用如图2表示,该反应的化学方程式为2H2S+SO2=3S+2H2O;