题目内容
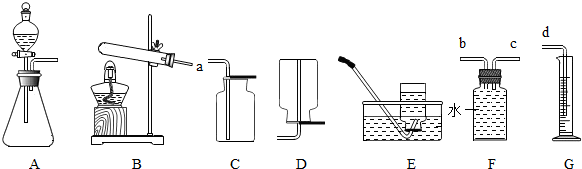
根据下列装置图回答问题:
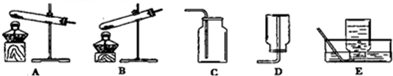
(1)某同学用氯酸钾和二氧化锰共热制备和收集氧气,他应选用的气体发生装置是
(2)被称为“绿色氧化剂”的过氧化氢(H2O2),俗称双氧水,是一种无色液体,常用作氧化剂、消毒杀菌剂和漂白剂等.在较低温度下和少量催化剂(如MnO2)条件下,它能迅速分解,生成氧气和水.请回答下列问题:
①写出图(1)中标号仪器的名称:b
②若实验室用过氧化氢代替氯酸钾制取氧气,可采用上面的哪种发生装置
③当过氧化氢接触二氧化锰后,反应便立即开始并不能人为控制其速度.如果稍改变你所选择的装置,便可控制其反应的速度.请从图2的仪器中选择一种仪器更换你选择的装置中的一种仪器,以达到控制反应速度的目的.你选择的仪器是
④天然气、沼气的主要成分是甲烷(CH4),它是无色无味的气体,密度比空气小,极难溶于水,能燃烧.实验室用无水醋酸钠和碱石灰固体混合物加热制取甲烷气体.若用此法制取甲烷气体,其气体发生装置选择 (从图1A、B、C中选择)
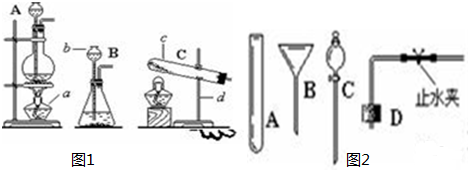
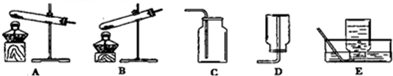
(1)某同学用氯酸钾和二氧化锰共热制备和收集氧气,他应选用的气体发生装置是
A
A
(填序号)来制取.用装置E来收集,其原因的氧气不易溶于水
氧气不易溶于水
,收集氧气的适宜时刻是当气泡连续且比较均匀放出时
当气泡连续且比较均匀放出时
.用文字表达式表示其化学反应氯酸钾
氯化钾+氧气
| 二氧化锰 |
| 加热 |
氯酸钾
氯化钾+氧气
.| 二氧化锰 |
| 加热 |
(2)被称为“绿色氧化剂”的过氧化氢(H2O2),俗称双氧水,是一种无色液体,常用作氧化剂、消毒杀菌剂和漂白剂等.在较低温度下和少量催化剂(如MnO2)条件下,它能迅速分解,生成氧气和水.请回答下列问题:
①写出图(1)中标号仪器的名称:b
酒精灯
酒精灯
; d长颈漏斗
长颈漏斗
.②若实验室用过氧化氢代替氯酸钾制取氧气,可采用上面的哪种发生装置
B
B
(填序号),主要理由是反应物是固体和液体,且反应在常温下进行
反应物是固体和液体,且反应在常温下进行
.③当过氧化氢接触二氧化锰后,反应便立即开始并不能人为控制其速度.如果稍改变你所选择的装置,便可控制其反应的速度.请从图2的仪器中选择一种仪器更换你选择的装置中的一种仪器,以达到控制反应速度的目的.你选择的仪器是
C
C
(填序号,下同),它更换原装置中的b
b
.控制反应速度的原理是:分液漏斗可以控制添加过氧化氢溶液的速度
分液漏斗可以控制添加过氧化氢溶液的速度
.④天然气、沼气的主要成分是甲烷(CH4),它是无色无味的气体,密度比空气小,极难溶于水,能燃烧.实验室用无水醋酸钠和碱石灰固体混合物加热制取甲烷气体.若用此法制取甲烷气体,其气体发生装置选择 (从图1A、B、C中选择)
C
C
;可采用排水法
排水法
或向下排空气法
向下排空气法
收集.
分析:(1)氯酸钾和二氧化锰共热制备氧气,属于固体加热型,故选发生装置A,氧气能用排水法收集是因为氧气不易溶于水,收集氧气的适宜时刻是气泡连续、均匀冒出时,并结合氯酸钾分解的反应原理书写表达式;
(2)①据常用仪器回答;
②用过氧化氢代替氯酸钾制取氧气,不需加热,属于固液常温型,故选发生装置B;
③要控制反应速率,则须控制反应物的浓度或反应物的量,可用分液漏斗代替长颈漏斗控制液体的滴加速度,进而达到控制反应速率的目的;
④据反应物状态和反应条件选择发生装置,据气体的密度好溶解性选择收集装置.
(2)①据常用仪器回答;
②用过氧化氢代替氯酸钾制取氧气,不需加热,属于固液常温型,故选发生装置B;
③要控制反应速率,则须控制反应物的浓度或反应物的量,可用分液漏斗代替长颈漏斗控制液体的滴加速度,进而达到控制反应速率的目的;
④据反应物状态和反应条件选择发生装置,据气体的密度好溶解性选择收集装置.
解答:解:(1)氯酸钾和二氧化锰共热制备氧气,属于固体加热型,故选发生装置A,氧气能用排水法收集是因为氧气不易溶于水,收集氧气的适宜时刻是气泡连续、均匀冒出时,氯酸钾在加热、二氧化锰作催化剂的条件下生成氯化钾和氧气,反应表达式是氯酸钾
氯化钾+氧气;
(2)①标号仪器分别是长颈漏斗和铁架台;
②用过氧化氢代替氯酸钾制取氧气,不需加热,属于固液常温型,故选发生装置B;
③要控制反应速率,则须控制反应物的浓度或反应物的量,可用分液漏斗代替长颈漏斗控制液体的滴加速度,进而达到控制反应速率的目的;
④用无水醋酸钠和碱石灰固体混合物加热制取甲烷气体属于固体加热型,故选发生装置C,甲烷的密度比空气小,极难溶于水,所以可用向下排空气法或排水法收集;
故答案为:(1)A; 氧气不易溶于水; 当气泡连续且比较均匀放出时;氯酸钾
氯化钾+氧气;
(2)①长颈漏斗; 铁架台;
②B; 反应物是固体和液体,且反应在常温下进行;
③C; b; 分液漏斗可以控制添加过氧化氢溶液的速度;
④C; 排水法; 向下排空气法.
| 二氧化锰 |
| 加热 |
(2)①标号仪器分别是长颈漏斗和铁架台;
②用过氧化氢代替氯酸钾制取氧气,不需加热,属于固液常温型,故选发生装置B;
③要控制反应速率,则须控制反应物的浓度或反应物的量,可用分液漏斗代替长颈漏斗控制液体的滴加速度,进而达到控制反应速率的目的;
④用无水醋酸钠和碱石灰固体混合物加热制取甲烷气体属于固体加热型,故选发生装置C,甲烷的密度比空气小,极难溶于水,所以可用向下排空气法或排水法收集;
故答案为:(1)A; 氧气不易溶于水; 当气泡连续且比较均匀放出时;氯酸钾
| 二氧化锰 |
| 加热 |
(2)①长颈漏斗; 铁架台;
②B; 反应物是固体和液体,且反应在常温下进行;
③C; b; 分液漏斗可以控制添加过氧化氢溶液的速度;
④C; 排水法; 向下排空气法.
点评:据反应物状态和反应条件选择发生装置,据气体的密度好溶解性选择收集装置,并了解常用仪器的用途,制取氧气的反应原理、收集方法、注意事项等知识.

练习册系列答案
相关题目