题目内容
40 g质量分数为36.5%的盐酸与25 g大理石恰好完全反应(大理石中的杂质不参加反应).
(1)计算该大理石中碳酸钙的质量分数.
(2)将40 g质量分数为36.5%的盐酸稀释为质量分数为10%的盐酸,需要水的质量是多少?
(1)设25g大理石中碳酸钙的质量为x, CaCO3+2HCl=CaCl2+H2O+CO2↑ 100 73 x 40g×36.5% 100 x = 73 40g×36.5% x=20g 大理石中碳酸钙的质量分数= 20g 25g ×100%=80% (2)设稀释后盐酸溶液的质量为y 40g×36.5%=y×10% y=146g 需要水的质量=146g-40g=106g 答:大理石中碳酸钙的质量分数为80%.将40g质量分数为36.5%的盐酸稀释为质量分数为10%的盐酸,需要水的质量是106g.

 优生乐园系列答案
优生乐园系列答案 实验室需配制一定浓度的硝酸钾溶液。
实验室需配制一定浓度的硝酸钾溶液。
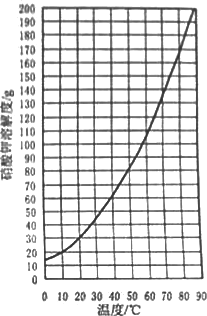
(1)查阅硝酸钾溶 解性。由右图可知,20 ℃时,硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数)。
解性。由右图可知,20 ℃时,硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数)。
(2)计算。配制40 g质量分数为10%的硝酸钾溶液,所需硝酸钾的质量为 g,所需蒸馏水的体积为 mL(水的密度近似看做1 g/mL)。
(3)称量。分别在天平左右两盘放上纸片,调节平衡后, (填字母)。
A.先移动游码到所需位置,再添加硝酸钾直到天平平衡
B.先添加所需的硝酸钾,再移动游码直到天平平衡
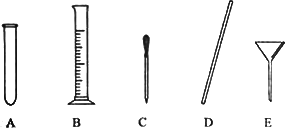
(4)量取。量取所需蒸馏水要用到的仪器是 (填字母)。

(5)溶解。将称量好的硝酸钾和蒸馏水混合溶解。
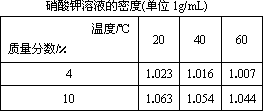
(6)稀释。20 ℃时,将20 mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液。从下表中找出需要用到的数据: g/mL。
硝酸钾溶液的密度(单位g/mL)
| 温度/℃ 质量分数/% | 20 | 40 | 60 |
| 4 | 1.023 | 1.016 | 1.007 |
| 10 | 1.063 | 1.054 | 1.044 |
 实验室需配制一定浓度的硝酸钾溶液。
实验室需配制一定浓度的硝酸钾溶液。
(1)查阅硝酸钾溶 解性。由右图可知,20 ℃时,硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数)。
解性。由右图可知,20 ℃时,硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数)。
(2)计算。配制40 g质量分数为10%的硝酸钾溶液,所需硝酸钾的质量为 g,所需蒸馏水的体积为 mL(水的密度近似看做1 g/mL)。
(3)称量。分别在天平左右两盘放上纸片,调节平衡后, (填字母)。
A.先移动游码到所需位置,再添加硝酸钾直到天平平衡
B.先添加所需的硝酸钾,再移动游码直到天平平衡
(4)量取。量取所需蒸馏水要用到的仪器是 (填字母)。
(5)溶解。将称量好的硝酸钾和蒸馏水混合溶解。
(6)稀释。20 ℃时,将20 mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液。从下表中找出需要用到的数据: g/mL。
硝酸钾溶液的密度(单位g/mL)
| 温度/℃ 质量分数/% | 20 | 40 | 60 |
| 4 | 1.023 | 1.016 | 1.007 |
| 10 | 1.063 | 1.054 | 1.044 |
 实验室需配制一定浓度的硝酸钾溶液。
实验室需配制一定浓度的硝酸钾溶液。
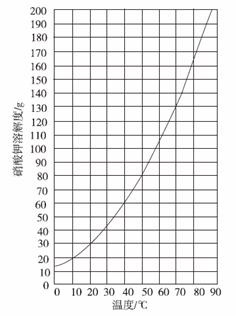
(1)查阅硝酸钾溶解性。由右图可知,20 ℃时, 硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数)。
硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数)。
(2)计算。配制40 g质量分数为10%的硝酸钾溶液,所需硝酸钾的质量为 g,所需蒸馏水的体积为 mL(水的密度近似看做1 g/mL) 。
。
(3)称量。分别在天平左右两盘放上纸片,调节平衡后, (填字母)。
A.先移动游码到所需位置,再添加硝酸钾直到天平平衡
B.先添加所需的硝酸钾,再移动游码直到天平平衡
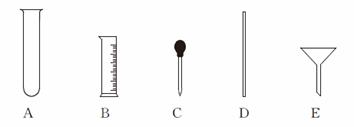
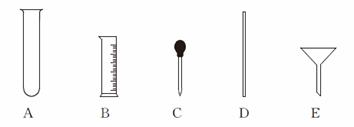
(4)量取。量取所需蒸馏水要用到的仪器是 (填字母)。
(5)溶解。将称量好的硝酸钾和蒸馏水混合溶解。
(6)稀释。20 ℃时,将20 mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液。从下表中找出需要用到的数据: g/mL。
硝酸钾溶液的密度(单位g/mL)
| 温度/℃ 质量分数/% | 20 | 40 | 60 |
| 4 | 1.023 | 1.016 | 1.007 |
| 10 | 1.063 | 1.054 | 1.044 |
实验室需配置一定浓度的硝酸钾溶液。
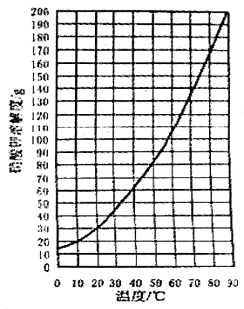 (1)查阅硝酸钾溶解性。由右图可知,20℃时,硝酸钾的溶解度为________g,在该温度下配制硝酸钾溶液,溶质质量分数最大为____%(计算结果保留整数)。
(1)查阅硝酸钾溶解性。由右图可知,20℃时,硝酸钾的溶解度为________g,在该温度下配制硝酸钾溶液,溶质质量分数最大为____%(计算结果保留整数)。
(2)计算。配制40 g质量分数为10%的硝酸钾溶液,所需硝酸钾质量为________g,所需蒸馏水的体积为________mL(水的密度近似看做l g/mL)。
(3)称量。分别在天平左右两盘放上纸片,调节平衡后, ________(填字母)。
A、先移动游码到所需位置,再添加硝酸钾直到天平平衡
B、先添加所需的硝酸钾,再移动游码直到天平平衡
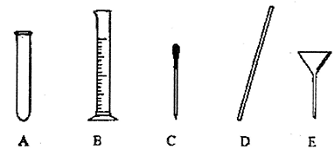
(4)量取。量取所需蒸馏水要用到 的仪器是____(填字母)。
的仪器是____(填字母)。
(5)溶解。将称量好的硝酸钾和蒸馏水混合溶解。
(6)稀释。20℃时,将20 mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液。从下表中找出需要用到的数据:____________g/mL。
硝酸钾溶液的密度(单位1 g/rnL)
| 温度℃ 质量分数/% | 20 | 40 | 60 |
| 4 | 1.023 | 1.016 | 1.007 |
| 10 | 1.063 | 1.054 | 1.004 |
(7) 20℃时,取哪份定质量的饱和硝酸钾溶液进行如下实验后,所得结论正确的是________。
A.保持温度不变,减少10 g溶剂后,溶液中溶质的质量分数增大
B.保持温度不变,加入10 g溶质后,溶液中溶质的质量分数增大
C.保持温度不变,加入10 g溶剂后,溶质的溶解度减小
D.降温至10℃后,溶质的溶解度减小