题目内容
 实验室需配制一定浓度的硝酸钾溶液。
实验室需配制一定浓度的硝酸钾溶液。
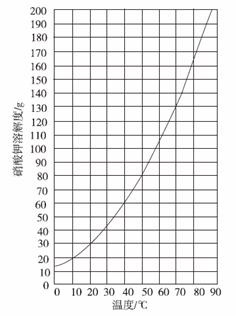
(1)查阅硝酸钾溶解性。由右图可知,20 ℃时, 硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数)。
硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数)。
(2)计算。配制40 g质量分数为10%的硝酸钾溶液,所需硝酸钾的质量为 g,所需蒸馏水的体积为 mL(水的密度近似看做1 g/mL) 。
。
(3)称量。分别在天平左右两盘放上纸片,调节平衡后, (填字母)。
A.先移动游码到所需位置,再添加硝酸钾直到天平平衡
B.先添加所需的硝酸钾,再移动游码直到天平平衡
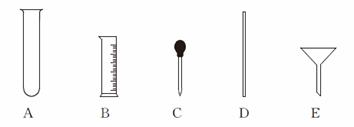
(4)量取。量取所需蒸馏水要用到的仪器是 (填字母)。
(5)溶解。将称量好的硝酸钾和蒸馏水混合溶解。
(6)稀释。20 ℃时,将20 mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液。从下表中找出需要用到的数据: g/mL。
硝酸钾溶液的密度(单位g/mL)
| 温度/℃ 质量分数/% | 20 | 40 | 60 |
| 4 | 1.023 | 1.016 | 1.007 |
| 10 | 1.063 | 1.054 | 1.044 |
(1)30 23 (2)4 36 (3)A (4)BC (6)1.063
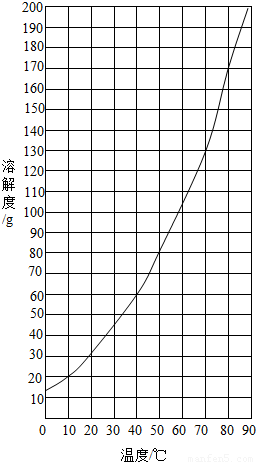
解析:(1)查硝酸钾的溶解度曲线,知20 ℃时,硝酸钾的溶解度为30 g,在该温度下配制硝酸钾溶液,其饱和溶液的溶质质量分数最大,为30 g/(100 g+30 g)×100%≈23%。(2)配制40 g质量分数为10%的硝酸钾溶液,所需硝酸钾质量为40 g×10%=4 g,所需蒸馏水的质量为40 g-4 g=36 g,因水的密度近似看做1 g/mL,故所需蒸馏水的体积为36 mL。(3)因为是称取一定量的固体药品,应先移动游码,再加药品至天平平衡,即选A。(4)量取一定体积的蒸馏水的方法是:先向量筒中倒入蒸馏水至接近36 mL刻度处,然后再把量筒放平,眼睛的视线与液体的凹液面保持水平,用胶头滴管滴加蒸馏水到36 mL刻度处,因此用到的仪器是量筒和胶头滴管,即选B、C。(6)计算时需要知道20 mL质量分数为10%的硝酸钾溶液的质量,因此需要用到10%的硝酸钾溶液的密度,即需要的数据是1.063 g/mL。

 黄冈创优卷系列答案
黄冈创优卷系列答案 实验室需配制一定浓度的硝酸钾溶液。
实验室需配制一定浓度的硝酸钾溶液。
(1)查阅硝酸钾溶 解性。由右图可知,20 ℃时,硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数)。
解性。由右图可知,20 ℃时,硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数)。
(2)计算。配制40 g质量分数为10%的硝酸钾溶液,所需硝酸钾的质量为 g,所需蒸馏水的体积为 mL(水的密度近似看做1 g/mL)。
(3)称量。分别在天平左右两盘放上纸片,调节平衡后, (填字母)。
A.先移动游码到所需位置,再添加硝酸钾直到天平平衡
B.先添加所需的硝酸钾,再移动游码直到天平平衡
(4)量取。量取所需蒸馏水要用到的仪器是 (填字母)。

(5)溶解。将称量好的硝酸钾和蒸馏水混合溶解。
(6)稀释。20 ℃时,将20 mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液。从下表中找出需要用到的数据: g/mL。
硝酸钾溶液的密度(单位g/mL)
| 温度/℃ 质量分数/% | 20 | 40 | 60 |
| 4 | 1.023 | 1.016 | 1.007 |
| 10 | 1.063 | 1.054 | 1.044 |
 实验室需配制一定浓度的硝酸钾溶液。
实验室需配制一定浓度的硝酸钾溶液。
(1)查阅硝酸钾溶 解性。由右图可知,20 ℃时,硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数)。
解性。由右图可知,20 ℃时,硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数)。
(2)计算。配制40 g质量分数为10%的硝酸钾溶液,所需硝酸钾的质量为 g,所需蒸馏水的体积为 mL(水的密度近似看做1 g/mL)。
(3)称量。分别在天平左右两盘放上纸片,调节平衡后, (填字母)。
A.先移动游码到所需位置,再添加硝酸钾直到天平平衡
B.先添加所需的硝酸钾,再移动游码直到天平平衡
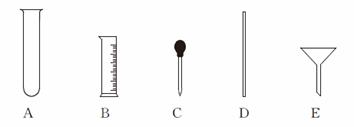
(4)量取。量取所需蒸馏水要用到的仪器是 (填字母)。
(5)溶解。将称量好的硝酸钾和蒸馏水混合溶解。
(6)稀释。20 ℃时,将20 mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液。从下表中找出需要用到的数据: g/mL。
硝酸钾溶液的密度(单位g/mL)
| 温度/℃ 质量分数/% | 20 | 40 | 60 |
| 4 | 1.023 | 1.016 | 1.007 |
| 10 | 1.063 | 1.054 | 1.044 |
 实验室需配制一定浓度的硝酸钾溶液.
实验室需配制一定浓度的硝酸钾溶液.
(1)查阅硝酸钾溶解性.由图1可知,20℃时,硝酸钾的溶解度为______g,在该温度下配制硝酸钾溶液,溶质质量分数最大为______%(计算结果保留整数).
(2)计算.配置40g质量分数为10%的硝酸钾溶液,所需硝酸钾质量为______g,所需蒸馏水的体积为______mL(水的密度近似看做1g/mL).
(3)称量.分别在天平左右两盘放上纸片,调节平衡后,______(填字母).
A、先移动游码到所需位置,再添加硝酸钾直到天平平衡
B、先添加所需的硝酸钾,再移动游码直到天平平衡
(4)量取.量取所需蒸馏水要用到的仪器是______(填字母)如图.
(5)溶解.将称量好的硝酸钾和蒸馏水混合溶解.
(6)稀释.20℃时,将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液.从下表中找出需要用到的数据:______g/mL.
硝酸钾溶液的密度(单位1g/mL)
| 温度/℃ 质量分数/% | 20 | 40 | 60 |
| 4 | 1.023 | 1.016 | 1.007 |
| 10 | 1.063 | 1.054 | 1.044 |
(1)查阅硝酸钾溶解性.由图1可知,20℃时,硝酸钾的溶解度为 g,在该温度下配制硝酸钾溶液,溶质质量分数最大为 %(计算结果保留整数).
(2)计算.配置40g质量分数为10%的硝酸钾溶液,所需硝酸钾质量为 g,所需蒸馏水的体积为 mL(水的密度近似看做1g/mL).
(3)称量.分别在天平左右两盘放上纸片,调节平衡后, (填字母).
A、先移动游码到所需位置,再添加硝酸钾直到天平平衡
B、先添加所需的硝酸钾,再移动游码直到天平平衡
(4)量取.量取所需蒸馏水要用到的仪器是 (填字母)如图.

(5)溶解.将称量好的硝酸钾和蒸馏水混合溶解.
(6)稀释.20℃时,将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液.从下表中找出需要用到的数据: g/mL.
硝酸钾溶液的密度(单位1g/mL)
| 温度/℃ 质量分数/% | 20 | 40 | 60 |
| 4 | 1.023 | 1.016 | 1.007 |
| 10 | 1.063 | 1.054 | 1.044 |
 (2013?广州)实验室需配制一定浓度的硝酸钾溶液.
(2013?广州)实验室需配制一定浓度的硝酸钾溶液.