题目内容
2.化学是一门以实验为基础的科学,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合下列实验装置图回答问题:
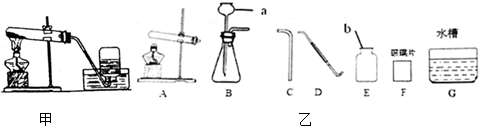
(1)写出指定仪器的名称:①试管②集气瓶
(2)实验室用氯酸钾和二氧化锰制取氧气应选用的反应装置是A(填字母代号),用排水法收集氧气完毕后,停止加热时的操作顺序是先把导管移出水面,然后熄灭酒精灯,以防止水倒吸进入热的试管中,造成试管破裂.
(3)双氧水(H2O2)是一种无色液体,常用于消毒、漂白等,加热到一定温度会放出氧气,而加入MnO2后,常温下可迅速分解,并生成水和氧气.写出用双氧水和二氧化锰制取氧气的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(4)实验室用大理石和稀盐酸制取二氧化碳应选用的反应装置是B(填字母代号),有关反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.收集二氧化碳通常用C装置,而不选用D或E装置,试从二氧化碳性质的角度来分析其原因相同条件下,二氧化碳气体的密度比空气大,且二氧化碳能溶于水(或能与水反应).
分析 (1)熟记仪器的名称;
(2)用氯酸钾和二氧化锰制取氧气的反应装置和反应原理:固体+固体,且需要加热,所以选用A装置;并回顾操作步骤:“查装定点收移熄”并要注意各步骤中的注意事项;
(3)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可;
(4)用大理石和稀盐酸制取二氧化碳的反应装置和反应原理:使用固体+液体反应,不需加热,所以可在B装置中进行;收集装置的选择主要利用气体的性质.
解答 解:(1)①是试管,②是集气瓶,故填:试管;集气瓶;
(2)用氯酸钾和二氧化锰制取氧气的反应装置和反应原理:固体+固体,且需要加热,所以选用A装置;在实验结束是,如果先停止加热再撤导管,
可能会由于试管内温度降低,压强变小而引起水的倒流引起试管炸裂,所以为了避免这种现象发生我们要:先撤导管,再停止加热.故填:A;把导管移出水面;熄灭酒精灯;
(3)过氧化氢在二氧化锰的催化作用下生成水和氧气,故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(4)用大理石和稀盐酸制取二氧化碳的反应装置和反应原理:使用固体+液体反应,不需加热,所以可在B装置中制取二氧化碳,其反应的化学方
程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑在选择气体的收集方法时,根据气体的水溶性和密度比空气是大还是小来选择收集方法,故由于二氧化碳的密度比空气大,能够溶于水,所以只能用向上排空气法收集,故用C装置来收集.
故填:B;CaCO3+2HCl═CaCl2+H2O+CO2↑;相同条件下,二氧化碳气体的密度比空气大,且二氧化碳能溶于水(或能与水反应).
点评 整理实验室制取氧气和二氧化碳的反应装置和反应原理,口诀记忆操作步骤和注意事项,并且熟记化学方程式.

 阅读快车系列答案
阅读快车系列答案| A. | 氢氧化钠溶液、稀盐酸 | B. | 氮气、氢气 | ||
| C. | 硝酸钡溶液、稀硫酸 | D. | 银、硝酸锌溶液 |
| A. | 塑料的合成 | B. | 橡胶的制造 | C. | 雪的消融 | D. | 化肥的制造 |
| A. | 氯cL | B. | 铜cu | C. | 硅SI | D. | 铁Fe |
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 4 | 1 | 42 | 10 |
| 反应后质量(g) | 4 | 20 | 6 | 待测 |
| A. | 该变化的基本反应类型一定是化合反应 | |
| B. | 丁反应后的质量为13克 | |
| C. | 反应中甲可能是催化剂 | |
| D. | 乙与丙的物质的量之比是19:36 |
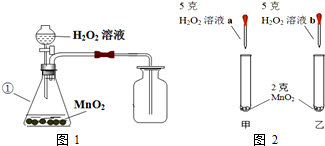
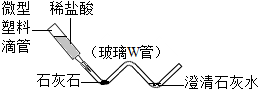
(1)写出编号为①的仪器名称:锥形瓶.
(2)某同学根据图2进行实验,观察到甲试管中产生气泡比乙试管中产生气泡多.你认为原因是a溶液比b溶液浓.
(3)20℃,市售的双氧水的浓度为10%,其中溶质和溶剂的质量比为1:9.取市售的20mL质量分数为10%的双氧水,加一定质量的水稀释成3%的双氧水.从如表中找出配制过程中需要用到的数据:1.024g/mL.最终可稀释得到68.3克3%的双氧水.(保留至0.01%)
| 溶质质量分数 | 10% | 3% |
| 密度(单位g/mL) | 1.024 | 0.991 |
①反应中生成氧气的质量为0.8g.
②根据化学方程式,计算该双氧水中溶质H2O2的质量.
③该双氧水的溶质质量分数为5%.
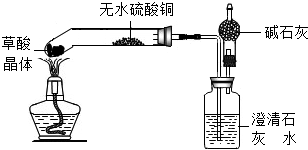 草酸的化学式为H2C2O4,某实验小组对草酸受热分解及其产物进行探究:
草酸的化学式为H2C2O4,某实验小组对草酸受热分解及其产物进行探究:【猜想与假设】猜想1:分解产物是 CO2、H2O
猜想2:分解产物是CO、H2O
猜想3:分解产物是CO2、CO
猜想4:分解产物是CO2、CO和H2O
根据质量守恒定律,以上猜想中,不可能的猜想是猜想3.
【查阅资料】(1)无水硫酸铜遇水由白色变成蓝色
(2)碱石灰(CaO和NaOH的混合物)是一种常用的干燥剂
(3)草酸晶体熔点较低,加热到182℃即可以熔化成液体
【实验设计】实验小组设计了如图的实验装置.
(注:①图中铁架台略去 ②装置中所用容器为底部弯曲的试管)
【实验过程】
| 实验操作 | 实验现象 | 实验结论 |
| 1.加热草酸晶体 | 无水硫酸铜变蓝色 | 说明有水(H2O)生成. |
| 澄清石灰水变浑浊 | 说明有二氧化碳(CO2)生成. | |
| 2.生成的气体通过碱石灰后,在干燥管的尖嘴处点燃,并在上方罩上内壁附着有澄清石灰水的小烧杯. | 气体燃烧,烧杯内壁的澄清石灰水变浑浊. | 说明有一氧化碳(CO);生成. |