题目内容
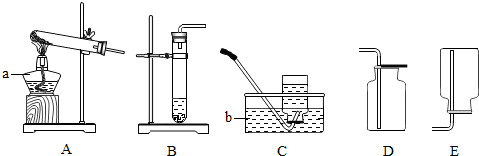
14.某化学兴趣小组通过查阅资料得知:固体草酸(H2C2O4•2H2O)受热可分解,其化学方程式为:H2C2O4•2H2O$\frac{\underline{\;\;△\;\;}}{\;}$CO↑+CO2↑+3H2O,该课题小组的同学在实验室分别进行了如下实验,回答下列问题:(1)甲同学利用如图装置制取并收集CO.

①试管口略向下倾斜的原因是防止水倒流,试管炸裂;
②B装置的作用除去二氧化碳(CO2).
(2)乙同学为了验证草酸的分解产物,设计了四个方案,分别将混合气体(包括水蒸气)依次通过足量的下列试剂:
A.石灰水、灼热的氧化铜、无水硫酸铜、氢氧化钠溶液
B.无水硫酸铜、氢氧化钠溶液、灼热的氧化铜、石灰水
C.石灰水、无水硫酸铜、灼热的氧化铜、石灰水
D.无水硫酸铜、石灰水、灼热的氧化铜、石灰水
其中正确的方案是D.
(3)丙同学按下列装置利用草酸分解产生的CO测定某种铁的氧化物的组成.

①丁同学认为去掉A装置,对测定结果无影响,他的观点不正确(填“正确”或“不正确”),判断理由是生成物中的CO2会影响测定结果.而戊同学认为从环保的角度考虑应在D装置后再增加尾气处理装置(点燃、收集等)装置,若无此装置,对测定结果是否有影响?否 (填“是”或“否”).
②当C装置中铁的氧化物全部被还原后,称量剩余的质量为11.2g,同时测得D装置的质量增加13.2g,则该铁的氧化物中铁元素和氧元素的质量比为7:3.
分析 (1)根据草酸分解的产物及所设计装置的目的,判断各装置的作用及操作注意事项;
(2)根据所设计方案中试剂在验证混合气体中的作用,设计正确的顺序对混合气体的每一成分进行验证;
(3)①分析为测定铁的氧化物的组成所设计的实验装置中各装置的作用,对各装置进行评价,并判断对测定结果所产生的影响;
②根据对所测得装置质量的分析,计算铁的氧化物中所含铁元素与氧元素的质量,求得该铁的氧化物中铁元素和氧元素的质量比.
解答 解:(1)①为防止在试管冷凝的水回流至试管底部而引起试管爆裂,在对固体物质加热时,试管口要略向下倾斜;
②利用氢氧化钠溶液吸收分解产物中的二氧化碳气体,从而收集到较为纯净的一氧化碳;
(2)由于检验二氧化碳气体需要把混合气体通入澄清石灰水,影响混合气体中水的检验,因此在检验二氧化碳、一氧化碳气体应首先使用无水硫酸铜检验混合气体中的水;然后利用澄清石灰水检验二氧化碳,而不能使用与二氧化碳反应无明显现象的氢氧化钠溶液,在检验一氧化碳前需要使用足量澄清石灰水既检验二氧化碳又完全吸收二氧化碳,接下来把气体通过灼热氧化铜和澄清石灰水,检验一氧化碳;故正确方案应选D方案;
(3)①装置A除去混合气体中的二氧化碳,若除去则会使所测得二氧化碳质量偏大;由于未完全反应一氧化碳会随尾气排入空气造成污染,因此需要对尾气进行收集或直接点燃的处理,该处理只是为防止造成空气污染,不影响测定结果;
②完全反应后,装置C中剩余固体质量11.2g即铁的氧化物中铁的质量,而装置D增加的质量为反应生成二氧化碳的质量,二氧化碳是由一氧化碳与氧化物中氧结合而得,因此二氧化碳中氧元素质量的一半为铁的氧化物中氧的质量,则铁的氧化物为氧的质量=13.2g×$\frac{32}{44}$×100%×$\frac{1}{2}$=4.8g;
则该铁的氧化物中铁元素和氧元素的质量比=11.2g:4.8g=7:3;
故答案为:
(1)①防止水倒流,试管炸裂;②除去二氧化碳(CO2);
(2);
(3)①不正确;生成物中的CO2会影响测定结果;尾气处理装置(点燃、收集等);否;②7:3.
点评 根据实验目的及所设计的实验装置,明确每个装置在实验中所起的作用,是解答好此问题的基础与关键.

 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案| A. | 在化学变化中,分子可分,而原子却不能再分 | |
| B. | 分子在不停地运动 | |
| C. | 分子由原子构成 | |
| D. | 分子的体积在变大 |
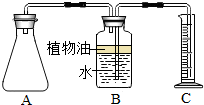 小明买了一种“汽泡爽”的冲调饮料.
小明买了一种“汽泡爽”的冲调饮料.(1)小明阅读资料发现:“汽泡爽”原料中的柠檬酸和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,请填写柠檬酸的化学式.
3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3CO2↑
(2)小明想探究加入的水的温度对产生气体量的影响,小明设计了如表实验方案.
| 实验序号 | 加入水的体积 | 加入水的温度 | 收集到的气体的体积 |
| 1 | 200mL | 15℃ | a(待记录) |
| 2 | 200mL | 50℃ | b(待记录) |
(3)通过实验,小明测得:a=64mL,b=132mL,由此获得结论:“汽泡爽”产生气体的量与加水温度有关系.但是老师看到小明的实验报告后却指出:两套装置中,“汽泡爽”产生气体的总量应该近似相等,与温度关系不大,其本质原因是温度高气体在水中的溶解度小,收集到的气体多.
(4)通过反思,为了证明老师的观点,小明继续利用(3)中已反应完的两套装置,又做了一步实验,发现两套装置最终收集到的气体的总量确实相近,他的实验操作是将装置1反应后的液体温度升高到50℃,继续收集气体并测量体积.
| A. | 乙>甲>丙 | B. | 乙>丙>甲 | C. | 丙>乙>甲 | D. | 乙>甲=丙 |
| A. | 圆底烧瓶 | B. | 烧杯 | C. | 燃烧匙 | D. | 锥形瓶 |