题目内容
13.金属材料应用广泛,如电路板中常用到焊锡、铜、银、铁等.(1)焊锡与其组成金属相比具有熔点低的特性,可用来焊接电子元件.
(2)将Cu片插入AgNO3溶液中,发生反应的化学方程式为Cu+2AgNO3═Cu(NO3)2+2Ag该反应属于置换反应 (填基本反应类型)
(3)若要验证Cu、Ag、Fe的活动性强弱,可选择的试剂组是C(填序号).
A.Fe、Cu、Ag、稀硫酸 B.Cu、Ag、FeSO4溶液 C.Fe、Ag、CuSO4溶液
(4)用金属活动顺序解释生活中的一些现象,如:不能用铁桶装酸液,因为在金属活动顺序表中铁排在氢前面能与酸反应,容器会受到腐蚀.不能用铁桶装硫酸铜溶液是因为在金属活动顺序表中铁排在铜的前面能与硫酸铜反应生成,容器会受到腐蚀.
分析 根据题干提供的信息结合金属活动性顺序的意义进行分析,在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此分析回答有关的问题.
解答 解:(1)焊锡与其组成金属相比具有熔点低的特性,可用来焊接电子元件.
(2)由于铜的金属活动性大于一银,所以将Cu片插入AgNO3溶液中,发生反应的化学方程式为:Cu+2AgNO3═Cu(NO3)2+2Ag,该反应是一种单质和一种化合物反应生成了另一种单质解另一种化合物,属于置换反应;
(3)A.由于Fe能与稀硫酸反应,Cu、Ag都不能与稀硫酸反应,能得出铁的活动性大于铜、银,但不能比较铜、银的活动性强弱,故A错误;
B.由于Cu、Ag都不能与与FeSO4溶液反应,只能得出铁的活动性大于铜、银,但不能比较铜、银的活动性强弱,故B错误;
C.Fe能与CuSO4溶液反应,Ag不能与CuSO4溶液反应,能得出Cu、Ag、Fe金属活动性强弱是Fe>Cu、>Ag,故C正确;
(4)用金属活动顺序解释生活中的一些现象,如:不能用铁桶装酸液,因为在金属活动顺序表中铁排在氢前面能与酸反应,容器会受到腐蚀.不能用铁桶装硫酸铜溶液是因为在金属活动顺序表中铁排在铜的前面能与硫酸铜反应生成,容器会受到腐蚀.
故答为:(1)熔点低;
(2)Cu+2AgNO3═Cu(NO3)2+2Ag,置换反应;
(3)不能用铁桶装酸液,因为在金属活动顺序表中铁排在氢前面能与酸反应,容器会受到腐蚀,不能用铁桶装硫酸铜溶液是因为在金属活动顺序表中铁排在铜的前面能与硫酸铜反应生成,容器会受到腐蚀.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案
相关题目
3. 向一定量CaCl2和HCl的混合溶液中,逐渐加入Na2CO3溶液,反应过程中产生气体或沉淀的质量与加入的Na2CO3溶液的质量关系如图,下列说法错误的是( )
向一定量CaCl2和HCl的混合溶液中,逐渐加入Na2CO3溶液,反应过程中产生气体或沉淀的质量与加入的Na2CO3溶液的质量关系如图,下列说法错误的是( )
 向一定量CaCl2和HCl的混合溶液中,逐渐加入Na2CO3溶液,反应过程中产生气体或沉淀的质量与加入的Na2CO3溶液的质量关系如图,下列说法错误的是( )
向一定量CaCl2和HCl的混合溶液中,逐渐加入Na2CO3溶液,反应过程中产生气体或沉淀的质量与加入的Na2CO3溶液的质量关系如图,下列说法错误的是( )| A. | OE发生化学反应:Na2CO3+2HCl═2NaCl+H2O+CO2↑ | |
| B. | PF有沉淀生成 | |
| C. | G点溶液的pH>7 | |
| D. | 反应过程有气体和沉淀生成,不遵循质量守恒定律 |
5. 在化学反应前后,物质所含元素化合价发生变化的反应属于氧化还原反应.氧化还原反应与四种基本反应类型间的关系如图所示,下列举例中错误的是( )
在化学反应前后,物质所含元素化合价发生变化的反应属于氧化还原反应.氧化还原反应与四种基本反应类型间的关系如图所示,下列举例中错误的是( )
 在化学反应前后,物质所含元素化合价发生变化的反应属于氧化还原反应.氧化还原反应与四种基本反应类型间的关系如图所示,下列举例中错误的是( )
在化学反应前后,物质所含元素化合价发生变化的反应属于氧化还原反应.氧化还原反应与四种基本反应类型间的关系如图所示,下列举例中错误的是( )| A. | 例1:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | B. | 例2:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | ||
| C. | 例3:Mg(OH)2+2HCl═MgCl2+2H2O | D. | 例4:Cu+2AgNO3═2Ag+Cu(NO3)2 |
2.关于下列实验现象,描述错误的是( )
| A. | 光亮的铜丝放入稀硫酸中,溶液变为蓝色,产生大量气泡 | |
| B. | 镁条在空气中剧烈燃烧,发出耀眼的白光,生成白色固体 | |
| C. | 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 氢气在空气中燃烧,产生淡蓝色火焰,放出大量的热 |
3.钛酸亚铁(FeTiO3)中铁元素显+2价,则钛元素的化合价是( )
| A. | +2 | B. | +3 | C. | +4 | D. | +5 |
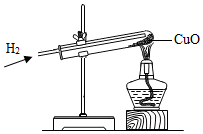 将氢气通入盛有氧化铜的试管中,加热一段时间后,可观察到试管中有红色固体出现.
将氢气通入盛有氧化铜的试管中,加热一段时间后,可观察到试管中有红色固体出现.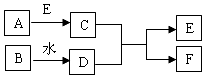 如图中A~F分别表示一种常见化合物,A、B都是氧化物,A通常为气态,F常用于实验室制取A(部分生成物已略去).
如图中A~F分别表示一种常见化合物,A、B都是氧化物,A通常为气态,F常用于实验室制取A(部分生成物已略去). 小明在市场看到,鱼老板将一勺白色粉末加入水中,水中奄奄一息的鱼很快张开嘴,活蹦乱跳起来,小明对这种“白色粉末”很感兴趣,与小刚进行了相关探究.
小明在市场看到,鱼老板将一勺白色粉末加入水中,水中奄奄一息的鱼很快张开嘴,活蹦乱跳起来,小明对这种“白色粉末”很感兴趣,与小刚进行了相关探究.