题目内容
17、碳酸钠和碳酸氢钠(NaHCO3)分别跟足量的盐酸反应(碳酸钠、碳酸氢钠分别跟盐酸反应,所得生成物相同),若要使这两个反应生成相等质量的二氧化碳,则所消耗碳酸钠与碳酸氢钠的质量比为
53:42
.分析:利用两物质与盐酸反应的化学方程式,让其生成相同量的二氧化碳,求两物质的质量比即可.
解答:解:让两个反应中都生成44份的二氧化碳,可求两物质的质量份数.
NaHCO3+HCl=NaCl+H2O+CO2↑
84 44
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
则两物质的质量比是:106:84=53:42
故答案为:53:42
NaHCO3+HCl=NaCl+H2O+CO2↑
84 44
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
则两物质的质量比是:106:84=53:42
故答案为:53:42
点评:此题是一道根据化学方程是计算的基础题,解题时可设生成的二氧化碳质量都是44,分别求出两物质的质量,然后球质量比即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目








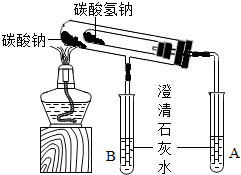 校兴趣小组对碳酸钠和碳酸氢钠的性质进一步研究,请你参与并完成相关问题.
校兴趣小组对碳酸钠和碳酸氢钠的性质进一步研究,请你参与并完成相关问题.