题目内容
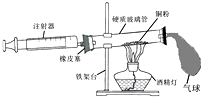
19.实验结束时,同学们将含有CuSO4、ZnSO4、FeSO4的废液倒在废液缸里,如果将废液直接排放就会造成水污染.于是几位同学利用课余处理废液,回收工业重要原料硫酸锌和有关金属.实验过程如下: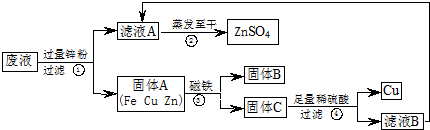
请回答:
(1)固体C的化学式为铜和锌.
(2)写出步骤①其中一个反应的化学方程式Zn+CuSO4=ZnSO4+Cu(或Zn+FeSO4═ZnSO4+Fe);步骤④发生反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑.
分析 在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,氢前的金属能与酸发生置换反应生成氢气,铁能被磁铁吸引,可以根据金属与酸的反应和金属与盐溶液的反应来进行固体的分离.
解答 解:(1)废液中含有硫酸铜、硫酸锌和硫酸亚铁,加入的过量锌粉能与与硫酸铜和硫酸亚铁反应,所以固体A中含有铁、铜和锌,铁能被磁铁吸引,所得的固体B为铁;固体C中含有铜和锌.
(2)由实验过程可知,步骤①中发生的反应有锌与硫酸铜和硫酸亚铁反应,反应的化学方程式为:Zn+CuSO4=ZnSO4+Cu;Zn+FeSO4═ZnSO4+Fe.固体C中含有铜和锌,剩余的锌与硫酸反应生成硫酸锌和氢气,所以反应的方程式是:Zn+H2SO4=ZnSO4+H2↑.
故答为:(1)铜和锌;(2)Zn+CuSO4=ZnSO4+Cu(或Zn+FeSO4═ZnSO4+Fe),Zn+H2SO4=ZnSO4+H2↑.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
9.下列实验操作正确的是( )
| A. | 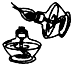 点燃酒精灯 | B. | 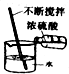 稀释浓硫酸 | C. | 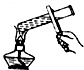 加热液体 | D. |  倾倒液体 |
14.某温度时,固体A的溶解度为25g.则在该温度下,A的饱和溶液中,溶质质量(a)、溶剂质量(b)和溶液质量(c)具有的关系是( )
| A. | c:b=4:5 | B. | a:c=l:5 | C. | a:b=l:3 | D. | b:c=3:4 |
4.实验室常用石灰石和稀盐酸制取二氧化碳.
探究一 气体发生装置的选择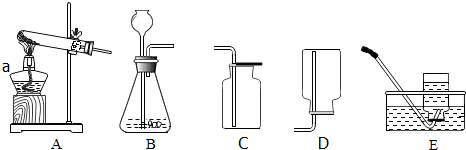
(1)写出图中仪器a的名称:酒精灯
(2)实验室制取二氧化碳气体,发生装置应选用B(填字母).二氧化碳验满的方法是把燃着木条放在集气瓶口,若燃着木条熄灭,则说明二氧化碳已收集满.
探究二 药品的选择
小明对三组药品进行了研究,实验记录如下.
对照实验①③,是探究药品的状态(或接触面积)对产生二氧化碳速率的影响;
对照实验①②,是探究不同的酸对产生二氧化碳速率的影响;小明选择第①组药品来制取二氧化碳,该组反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.
探究三 验证生成的气体
将生成的气体通入澄清的石灰水,若澄清的石灰水变浑浊,则证明生成的气体是二氧化碳.该反应的化学方程式:CO2+Ca(OH)2═CaCO3↓+H2O.
探究一 气体发生装置的选择

(1)写出图中仪器a的名称:酒精灯
(2)实验室制取二氧化碳气体,发生装置应选用B(填字母).二氧化碳验满的方法是把燃着木条放在集气瓶口,若燃着木条熄灭,则说明二氧化碳已收集满.
探究二 药品的选择
小明对三组药品进行了研究,实验记录如下.
| 组 别 | 药 品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡的速率缓慢并逐渐停止 |
| ③ | 粉末状石灰石和稀盐酸 | 产生气泡的速率很快 |
对照实验①②,是探究不同的酸对产生二氧化碳速率的影响;小明选择第①组药品来制取二氧化碳,该组反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.
探究三 验证生成的气体
将生成的气体通入澄清的石灰水,若澄清的石灰水变浑浊,则证明生成的气体是二氧化碳.该反应的化学方程式:CO2+Ca(OH)2═CaCO3↓+H2O.
8.下列属于纯净物的有( )
| A. | 空气 | B. | 稀有气体 | ||
| C. | 过氧化氢溶液 | D. | 磷在氧气中燃烧后的生成物 |