题目内容
17.有一表面被氧化的镁条8克,与足量的稀盐酸完全反应,产生氢气0.2克,求:(1)镁条中的氧化镁的质量是多少克?
(2)镁条中镁的质量分数是多少?
(3)反应后生成溶质的质量是多少?
分析 镁和稀盐酸反应生成氯化镁和氢气,氧化镁和稀盐酸反应生成氯化镁和水,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)设镁的质量为x,和稀盐酸反应生成氯化镁质量为y,
Mg+2HCl═MgCl2+H2↑,
24 95 2
x y 0.2g
$\frac{24}{x}$=$\frac{95}{y}$=$\frac{2}{0.2g}$,
x=2.4g,y=9.5g,
氧化镁质量为:8g-2.4g=5.6g,
答:氧化镁质量是5.6g.
(2)镁条中镁的质量分数是:$\frac{2.4g}{8g}$×100%=30%,
答:镁条中镁的质量分数是30%.
(3)设氧化镁和稀盐酸反应生成氯化镁质量为z,
MgO+2HCl═MgCl2+H2O,
40 95
5.6g z
$\frac{40}{5.6g}$=$\frac{95}{z}$,
z=13.3g,
反应后生成溶质的质量是:9.5g+13.3g=22.8g,
答:反应后生成溶质的质量是22.8g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
7.生活中处处存在着化学知识,下列过程中属于化学变化的是( )
| A. | 家庭自制冰块 | |
| B. | 烧菜用过的铁锅放置后常出现红色斑迹 | |
| C. | 夏天轮胎容易爆胎 | |
| D. | 用酒精棉球给发热病人擦拭降温 |
5.如图是用铜粉氧化法生产氧化铜的流程图.据图回答下列问题:
 (1)铜粉灼烧后可能有氧化铜和氧化亚铜两种物质.氧化亚铜(Cu2O)中铜元素的化合价是+1价.
(1)铜粉灼烧后可能有氧化铜和氧化亚铜两种物质.氧化亚铜(Cu2O)中铜元素的化合价是+1价.
(2)已知氧化亚铜和稀硫酸反应可生成硫酸铜和铜.
假如固体1中只含有铜的氧化物,下列推理合理的是②(填序号).
①固体1中加入稀硫酸,若溶液呈蓝色,说明该固体中一定有氧化铜
②固体1中加入稀硫酸,若有红色沉淀物,说明该固体中一定有氧化亚铜
(3)若用贴有如图标签的浓硫酸100毫升可配制溶质质量分数为20%的硫酸溶液多少克?
 (1)铜粉灼烧后可能有氧化铜和氧化亚铜两种物质.氧化亚铜(Cu2O)中铜元素的化合价是+1价.
(1)铜粉灼烧后可能有氧化铜和氧化亚铜两种物质.氧化亚铜(Cu2O)中铜元素的化合价是+1价.(2)已知氧化亚铜和稀硫酸反应可生成硫酸铜和铜.
假如固体1中只含有铜的氧化物,下列推理合理的是②(填序号).
①固体1中加入稀硫酸,若溶液呈蓝色,说明该固体中一定有氧化铜
②固体1中加入稀硫酸,若有红色沉淀物,说明该固体中一定有氧化亚铜
(3)若用贴有如图标签的浓硫酸100毫升可配制溶质质量分数为20%的硫酸溶液多少克?
| 硫酸(500mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84g/cm3 溶质质量分数:98% |
6.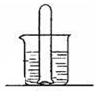 如图所示,烧杯中装有澄清石灰水,某同学把一支充满二氧化碳气体的试管倒插在烧杯中一段时间后,则下列说法正确的是( )
如图所示,烧杯中装有澄清石灰水,某同学把一支充满二氧化碳气体的试管倒插在烧杯中一段时间后,则下列说法正确的是( )
 如图所示,烧杯中装有澄清石灰水,某同学把一支充满二氧化碳气体的试管倒插在烧杯中一段时间后,则下列说法正确的是( )
如图所示,烧杯中装有澄清石灰水,某同学把一支充满二氧化碳气体的试管倒插在烧杯中一段时间后,则下列说法正确的是( )| A. | 无明显现象 | |
| B. | 烧杯中溶液变浑浊 | |
| C. | 试管内液面上升 | |
| D. | 该实验说明了二氧化碳气体密度比空气大 |
 “开车不喝酒,喝酒不开车”.因为酒后驾车出事多,就专门为警察设计的一款执法的检测工具--酒精检测仪,根据酒精浓度和血液中酒精浓度会呈现出一定比例关系的原理,通过测定驾驶者的呼气,很快计算出受测者血液中的酒精含量.用来对饮酒司机的饮酒多少来进行具体的处理,有效减少重大交通事故的发生.其原理是:把呈黄色的酸化的三氧化铬(CrO3)载带在硅胶上,它是一种强氧化剂,而人体呼出的乙醇(酒精)具有还原性,两者发生以下反应:2CrO3+3C2H5OH+3H2SO4═Cr2(SO4)3+3CH3CHO+6H2O 生成物硫酸铬是蓝绿色的.通过这一颜色变化,可据此检测酒精蒸气.根据这些,请回答下列问题:
“开车不喝酒,喝酒不开车”.因为酒后驾车出事多,就专门为警察设计的一款执法的检测工具--酒精检测仪,根据酒精浓度和血液中酒精浓度会呈现出一定比例关系的原理,通过测定驾驶者的呼气,很快计算出受测者血液中的酒精含量.用来对饮酒司机的饮酒多少来进行具体的处理,有效减少重大交通事故的发生.其原理是:把呈黄色的酸化的三氧化铬(CrO3)载带在硅胶上,它是一种强氧化剂,而人体呼出的乙醇(酒精)具有还原性,两者发生以下反应:2CrO3+3C2H5OH+3H2SO4═Cr2(SO4)3+3CH3CHO+6H2O 生成物硫酸铬是蓝绿色的.通过这一颜色变化,可据此检测酒精蒸气.根据这些,请回答下列问题: