题目内容
向盛有一定质量的NaCl和Na2SO4固体混合物的烧杯中加水,固体完全溶解后,再加入一定质量分数的BaCl2溶液至恰好完全反应,过滤烘干得到23.3g沉淀,经测定滤液中含有氯元素的质量为21.3g(不考虑过程中物质质量的损失),计算原固体混合物中NaCl的质量为( )
| A、5.85g |
| B、11.7g |
| C、14.2g |
| D、23.4g |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:向氯化钠和硫酸钠的混合溶液中加入氯化钡溶液,氯化钡和硫酸钠发生反应生成硫酸钡沉淀.
滤液中的氯化钠包括原混合物中的氯化钠和反应生成的氯化钠,根据氯元素的质量求出滤液中氯化钠的总质量,再用氯化钠的总质量-反应生成的氯化钠的质量(可根据硫酸钡的质量求出)即可求出原混合物中氯化钠的质量.
滤液中的氯化钠包括原混合物中的氯化钠和反应生成的氯化钠,根据氯元素的质量求出滤液中氯化钠的总质量,再用氯化钠的总质量-反应生成的氯化钠的质量(可根据硫酸钡的质量求出)即可求出原混合物中氯化钠的质量.
解答:解:
设生成氯化钠的质量为x
Na2SO4+BaCl2═2NaCl+BaSO4↓
117 233
x 23.3g
=
x=11.7g
滤液中氯化钠的质量=21.3g÷
×100%=35.1g
原固体混合物中NaCl的质量为35.1g-11.7g=23.4g
答案:D
设生成氯化钠的质量为x
Na2SO4+BaCl2═2NaCl+BaSO4↓
117 233
x 23.3g
| 117 |
| 233 |
| x |
| 23.3g |
x=11.7g
滤液中氯化钠的质量=21.3g÷
| 35.5 |
| 58.5 |
原固体混合物中NaCl的质量为35.1g-11.7g=23.4g
答案:D
点评:本道题有两个突破点:一是根据复分解反应的条件判断是哪些物质在发生反应;二是涉及到有关化学式的计算.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
下列生活中或实验室的物质,属于纯净物的是( )
| A、冰啤酒 | B、新鲜空气 |
| C、优质燃煤 | D、蒸馏水 |
下列物质的化学式书写错误的是( )
| A、氯化钠 NaCl |
| B、氧化铝 AlO |
| C、氢氧化铁 Fe(OH)3 |
| D、硫酸铜 CuSO4 |
下列物质属于纯净物的是( )
| A、凉茶 | B、冰水 | C、空气 | D、大理石 |
化学科学的发展促进了人类社会文明的进步,化学已日益渗透到社会生活的各个方面.你认为下列各项不属于化学学科基本观念的是( )
| A、物质变化的观念 |
| B、物质运动的观念 |
| C、物质都是由元素组成的观念 |
| D、物质都是由微小粒子构成的观念 |
人体健康离不开化学.下列叙述错误的是( )
| A、海产品、瘦肉、肝脏含有丰富的人体所需的锌元素 |
| B、铁、碘、钾、钠、镁是人体所需的常量元素 |
| C、霉变的食物中含有黄曲霉毒素,不能食用 |
| D、人体氟过量会引起氟骨病,氟元素缺乏会导致龋齿 |
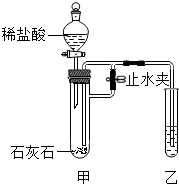 某化学小组在课外活动时做了一个实验,在甲试管中装入固体物质,乙试管中装入试剂溶液,按如图所示组装好仪器(图中铁架台等仪器已略去).通过分液漏斗加入足量稀盐酸,同时打开止水夹,看到乙试管液体中有气泡冒出;再关闭止水夹,发现-段时间后乙中溶液变浑浊.符合此实验现象的是( )
某化学小组在课外活动时做了一个实验,在甲试管中装入固体物质,乙试管中装入试剂溶液,按如图所示组装好仪器(图中铁架台等仪器已略去).通过分液漏斗加入足量稀盐酸,同时打开止水夹,看到乙试管液体中有气泡冒出;再关闭止水夹,发现-段时间后乙中溶液变浑浊.符合此实验现象的是( )

 构建知识网络是一种重要的学习方法,如图是关于E物质的知识网络,E物质是海洋中最多的一种物质,C物质的组成元素与E完全相同,D物质存在于汽水中,B物质是一种单质,具有助燃性;A物质组成元素中含有金属元素(注意:反应条件、部分反应物和生成物没有给出).
构建知识网络是一种重要的学习方法,如图是关于E物质的知识网络,E物质是海洋中最多的一种物质,C物质的组成元素与E完全相同,D物质存在于汽水中,B物质是一种单质,具有助燃性;A物质组成元素中含有金属元素(注意:反应条件、部分反应物和生成物没有给出).