题目内容
17.在用稀盐酸和氢氧化钠溶液进行中和反应的实验时,回答下列问题:(1)该反应的化学方程式为NaOH+HCl=NaCl+H2O.
(2)当把氢氧化钠溶液加入稀盐酸,还没有完全反应时溶液中的溶质为(写化学式)HCl、NaCl.
(3)当加入氢氧化钠溶液过量时,向所得溶液中滴加酚酞试液,溶液呈红色.
分析 (1)根据化学方程式的书写方法写出化学方程式;(2)当把氢氧化钠溶液加入稀盐酸,还没有完全反应时,盐酸没被中和完,所以盐酸过量,溶质中含有氯化钠和氯化氢;(3)当加入氢氧化钠溶液过量时,溶液显碱性,能使酚酞试液变红色.
解答 解:(1)反应物是盐酸和氢氧化钠,生成物是氯化钠和水,所以方程式是:NaOH+HCl=NaCl+H2O;
(2)当把氢氧化钠溶液加入稀盐酸,还没有完全反应时,盐酸没被中和完,所以盐酸过量,溶质中含有氯化钠和氯化氢;
(3)当加入氢氧化钠溶液过量时,溶液显碱性,能使酚酞试液变红色.
故答案为:(1)NaOH+HCl=NaCl+H2O;(2)HCl、NaCl;(3)红.
点评 解答本题关键是知道方程式的书写方法,判断反应后溶质时,不仅考虑生成物,还需要考虑反应物是否过量问题.

练习册系列答案
相关题目
15.某食品厂加工生产的将有中氯化钠的质量分数为15%~18%,该厂日产酱油15t,则该厂每月(按30天计)消耗氯化钠的质量至少为( )
| A. | 67.5t | B. | 13.80t | C. | 73.75t | D. | 22.5t |
5.分别将下列各组物质同时加到水中,能大量共存的是( )
| A. | NaCl、AgNO3、Na2SO4 | B. | Na2SO4、KNO3、NaOH | ||
| C. | H2SO4、NaCI、BaCl2 | D. | FeCl3、NaCl、KOH |
9.生活中一些物质pH如图所示,下列有关说法正确的( )
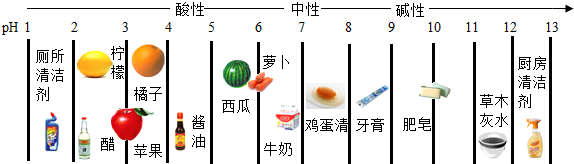

| A. | 草木灰水显碱性农民可把它和碳铵混合一起用 | |
| B. | 胃酸过多的人不宜多吃柠檬橘子 | |
| C. | 为增强洗涤效果可将厕所清洁剂和厨房清洁剂混合使用 | |
| D. | 食醋可使石蕊溶液变蓝也可除水垢 |
7.下列设计的实验方案中不能达到目的是( )
| A. | 除去CaCl2溶液中的HCl最好用CaCO3 | |
| B. | 用稀盐酸区分铁粉和木炭粉 | |
| C. | NaOH 溶液区分CO和CO2 | |
| D. | 用水区分NaCl、NaOH、NH4NO3 |