题目内容
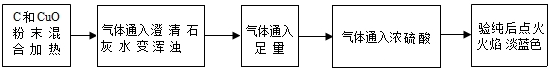
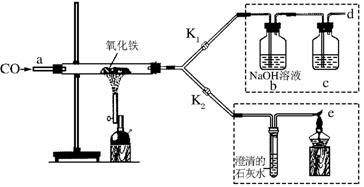
某同学对课本中C和CuO反应的产物进行了进一步的探究,以下是进行实验的部分流程(装置省略,且气密性好)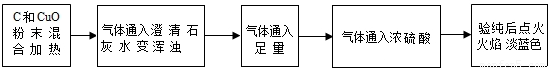
取出反应后的固体,观察呈红色
《查阅资料》C也能将CuO还原为红色的Cu2O Cu2O+H2SO4═Cu+CuSO4+H2O
《猜想》a 红色固体只是Cu b 红色固体是 c 红色固体是Cu和Cu2O混合物
实验探究
| 实验操作 | 实验现象 | 实验结论 |
| 取7.2克红色固体,置于烧杯中,向其中加入足量的稀硫酸,充分搅拌,静置 | 无明显现象 | (1)证明红色固体是 |
| (2) (填现象) | (3)证明红色固体肯定含 | |
| 取上述反应液过滤、洗涤、干燥和称量,得固体6.8克 | / | (4)Cu2O有 克 |
【答案】分析:【猜想】根据C在高温条件与CuO反应可生成红色Cu或Cu2O,可猜想反应后的红色固体为Cu或Cu2O之一或两者都有;
【实验探究】红色固体若为Cu,放入硫酸中因不能反应而无明显现象;红色固体若为Cu2O,放入硫酸中会发生反应生成铜、硫酸铜和水,观察到红色固体部分溶解且溶液变成蓝色;根据以上性质及变化时现象的不同,可使用硫酸检验红色固体的组成;
通过假设所取固体全部为Cu2O计算出与硫酸反应后可生成铜的质量,并与实验结果对比,判断红色固体的组成.
解答:解:【猜想】C在高温条件与CuO反应可生成红色Cu或Cu2O,所以,反应后得到的红色固体可能是铜,也可能是氧化亚铜,还可能为铜与氧化亚铜的混合物;故可猜测红色固体为:红色固体只是Cu2O;
【实验探究】根据铜不能与稀硫酸反应而Cu2O却可与稀硫酸生成铜、硫酸铜和水,把红色固体放入稀硫酸中,无明显变化时,红色固体全部为铜;
若观察到红色固体部分消失且反应后的溶液呈蓝色,红色固体一定含有Cu2O;
设混合物中含有氧化亚铜的质量为x
则:Cu2O+H2SO4═Cu+CuSO4+H2O 固体减少的质量
144 64 144-64=80
x 7.2g-6.8g=0.4g
 =
=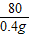
解得:x=0.72g
故答案为:【猜想】Cu2O;
【实验探究】
点评:解答这类题目时,首先,赏析问题情景,找到实验探究的反应原理,以及计算所要用到的数据;再根据实验的反应原理,利用所称取的样品进行实验探究,分析推断出该物质的组成成分.
【实验探究】红色固体若为Cu,放入硫酸中因不能反应而无明显现象;红色固体若为Cu2O,放入硫酸中会发生反应生成铜、硫酸铜和水,观察到红色固体部分溶解且溶液变成蓝色;根据以上性质及变化时现象的不同,可使用硫酸检验红色固体的组成;
通过假设所取固体全部为Cu2O计算出与硫酸反应后可生成铜的质量,并与实验结果对比,判断红色固体的组成.
解答:解:【猜想】C在高温条件与CuO反应可生成红色Cu或Cu2O,所以,反应后得到的红色固体可能是铜,也可能是氧化亚铜,还可能为铜与氧化亚铜的混合物;故可猜测红色固体为:红色固体只是Cu2O;
【实验探究】根据铜不能与稀硫酸反应而Cu2O却可与稀硫酸生成铜、硫酸铜和水,把红色固体放入稀硫酸中,无明显变化时,红色固体全部为铜;
若观察到红色固体部分消失且反应后的溶液呈蓝色,红色固体一定含有Cu2O;
设混合物中含有氧化亚铜的质量为x
则:Cu2O+H2SO4═Cu+CuSO4+H2O 固体减少的质量
144 64 144-64=80
x 7.2g-6.8g=0.4g
 =
=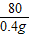
解得:x=0.72g
故答案为:【猜想】Cu2O;
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 取7.2克红色固体,置于烧杯中,向其中加入足量的稀硫酸,充分搅拌,静置 | 无明显现象 | (1)证明红色固体是 Cu |
| (2)溶液变成蓝色 (填现象) | (3)证明红色固体肯定含 Cu2O | |
| 取上述反应液过滤、洗涤、干燥和称量,得固体6.8克 | / | (4)Cu2O有 0.72克 |
点评:解答这类题目时,首先,赏析问题情景,找到实验探究的反应原理,以及计算所要用到的数据;再根据实验的反应原理,利用所称取的样品进行实验探究,分析推断出该物质的组成成分.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
有一种矿石称为“孔雀石”,它有孔雀羽毛般绿色斑纹,它的主要成分是碱式碳酸铜[Cu2(OH)2CO3].因碱式碳酸铜中含有铜元素,某兴趣小组同学对如何从孔雀石中提炼金属铜产生了浓厚兴趣,为此采集了适量的孔雀石样品,在老师的指导下进行了下列探究活动.
(1)经查阅资料,已知碱式碳酸铜具有下列性质,你认为其中属于化学性质的是______.
A.绿色固体B.不溶于水C.加热碱式碳酸铜会生成水、二氧化碳和氧化铜
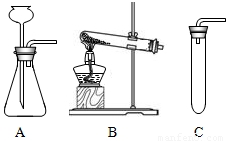
(2)加热孔雀石样品使之分解,应选用下列______(填装置的序号)装置,其理由是______.
(3)检验生成的气体中是否含有CO2需要用到的化学试剂名称是______;观察到______时,证明实验中有CO2产生.
(4)选用课本“木炭还原氧化铜”装置进行实验时,得到红色固体,一般认为是金属铜.但资料也表明,C也能将CuO还原为红色固体Cu2O(氧化亚铜);Cu2O+H2SO4=Cu+CuSO4+H2O.试与兴趣小组同学合作完成进一步确认红色固体成分的实验报告
(1)经查阅资料,已知碱式碳酸铜具有下列性质,你认为其中属于化学性质的是______.
A.绿色固体B.不溶于水C.加热碱式碳酸铜会生成水、二氧化碳和氧化铜
(2)加热孔雀石样品使之分解,应选用下列______(填装置的序号)装置,其理由是______.
(3)检验生成的气体中是否含有CO2需要用到的化学试剂名称是______;观察到______时,证明实验中有CO2产生.
(4)选用课本“木炭还原氧化铜”装置进行实验时,得到红色固体,一般认为是金属铜.但资料也表明,C也能将CuO还原为红色固体Cu2O(氧化亚铜);Cu2O+H2SO4=Cu+CuSO4+H2O.试与兴趣小组同学合作完成进一步确认红色固体成分的实验报告
| 实 验 操 作 | 现 象 | 分析 |
| 取7.2g红色固体,置于烧杯中,向其中加入足量稀硫酸,充分搅拌,静置. | 若无变化现象. | 证明红色固体是______. |
| 若有______. | 证明红色固体肯定含有______. | |
| 取上述反应后的溶液过滤、洗涤、干燥和称量,得固体6.8g. | -------------- | 确认红色固体是______. |