题目内容
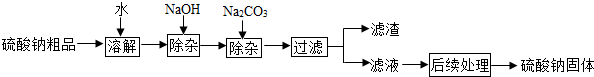
硫酸钠是制造纸浆、染料稀释剂、医药品等的重要原料.某硫酸钠粗品中含有少量CaCl2和MgCl2,实验室进行提纯的流程如下:

回答下列问题:
(1)用NaOH和Na2CO3除杂时,反应的化学方程式分别为:________、________.
(2)NaOH和Na2CO3如果添加过量了,可加入适量________溶液除去.
(3)“后续处理”的主要操作是蒸发,为了获得纯净的硫酸钠,应蒸发至________(填序号).
A.完全蒸干时停止加热
B.快干时停止加热,利用余热蒸干
C.有大量固体析出时停止加热,过滤弃去剩余的少量溶液
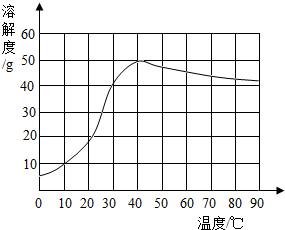
(4)已知硫酸钠的溶解度随温度变化的曲线如下图所示.
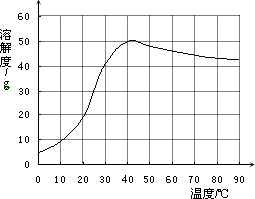
则40℃时,100 g蒸馏水中溶解________g硫酸钠达到饱和.将该饱和溶液升高温度至90℃,观察到的现象是________.
答案:
解析:
解析:
(1)2NaOH+MgCl2=Mg(OH)2↓+2NaCl(2
分) Na2CO3+CaCl2=CaCO3↓+2NaCl(2分)(2)H2SO4(1
分)(3)C(1
分)(4)50(1
分) 有固体(或晶体)析出(1分)
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 A.完全蒸干时停止加热
A.完全蒸干时停止加热



