题目内容
下列实验装置常用于实验室制取气体,根据给出的装置回答下列问题:
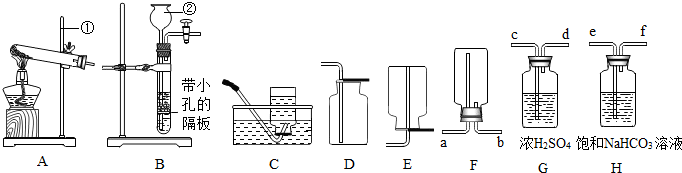
(1)指出编号仪器名称:① ;
(2)实验室利用A装置制取氧气,反应原理用化学方程式表示为 .
(3)制取二氧化碳应选择B装置突出优点是 ,该反应原理用化学方程式表示为 ;制得的二氧化碳中常含有少量的氯化氢气体与水蒸气,欲使用G、H装置将以上杂质气体除去,则装置正确的连接顺序是:混合气体→ (用端口字母表示).

(1)指出编号仪器名称:①
(2)实验室利用A装置制取氧气,反应原理用化学方程式表示为
(3)制取二氧化碳应选择B装置突出优点是
考点:常用气体的发生装置和收集装置与选取方法,气体的净化(除杂),实验室制取氧气的反应原理,二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)要熟悉各种仪器的名称、用途;
(2)A装置是加热固体制取气体的装置,且试管口无棉花,说明是用加热氯酸钾和二氧化锰混合物的方法制取氧气,据反应原理书写方程式;
(3)利用有孔隔板、可通过夹子的开闭控制反应的发生和停止,据反应原理书写方程式;如果需要除去氯化氢和水时,一般应该先除去氯化氢,后除去水.
(2)A装置是加热固体制取气体的装置,且试管口无棉花,说明是用加热氯酸钾和二氧化锰混合物的方法制取氧气,据反应原理书写方程式;
(3)利用有孔隔板、可通过夹子的开闭控制反应的发生和停止,据反应原理书写方程式;如果需要除去氯化氢和水时,一般应该先除去氯化氢,后除去水.
解答:解:(1)①是铁架台;
(2)A装置是加热固体制取气体的装置,且试管口无棉花,说明是用加热氯酸钾和二氧化锰混合物的方法制取氧气,氯酸钾在二氧化锰的催化作用下受热分解生成氯化钾和氧气,反应的化学方程式为:2KClO3
2KCl+3O2↑;
(3)制取二氧化碳用大理石和稀盐酸常温反应,不需要加热,属于固液常温型,发生装置选B,使用该套装置制取气体的突出优点是:可通过夹子的开闭控制反应的发生和停止,打开夹子,固液接触产生气体,关闭夹子,试管内压强增大,将液体压入长颈漏斗,固液分离,反应停止;
实验室用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石或石灰石的主要成分是碳酸钙,碳酸钙和稀盐酸反应能生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
要除去氯化氢气体与水蒸气,应该先通过饱和的碳酸氢钠溶液除去氯化氢,再通过浓硫酸除去水,因为气体通过碳酸氢钠溶液会带来水蒸气;
故答案为:(1)铁架台;(2)2KClO3
2KCl+3O2↑;(3)便于控制反应的发生与停止;CaCO3+2HCl═CaCl2+H2O+CO2↑; e→f→c→d.
(2)A装置是加热固体制取气体的装置,且试管口无棉花,说明是用加热氯酸钾和二氧化锰混合物的方法制取氧气,氯酸钾在二氧化锰的催化作用下受热分解生成氯化钾和氧气,反应的化学方程式为:2KClO3
| ||
| △ |
(3)制取二氧化碳用大理石和稀盐酸常温反应,不需要加热,属于固液常温型,发生装置选B,使用该套装置制取气体的突出优点是:可通过夹子的开闭控制反应的发生和停止,打开夹子,固液接触产生气体,关闭夹子,试管内压强增大,将液体压入长颈漏斗,固液分离,反应停止;
实验室用大理石或石灰石和稀盐酸反应制取二氧化碳,大理石或石灰石的主要成分是碳酸钙,碳酸钙和稀盐酸反应能生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
要除去氯化氢气体与水蒸气,应该先通过饱和的碳酸氢钠溶液除去氯化氢,再通过浓硫酸除去水,因为气体通过碳酸氢钠溶液会带来水蒸气;
故答案为:(1)铁架台;(2)2KClO3
| ||
| △ |
点评:本题主要考查实验设计、杂质去除和化学方程式的书写等方面的知识,能较好考查学生对知识的掌握和应用能力.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
下列实验现象中不正确的是( )
| A、铁丝在氧气中燃烧火星四射,生成黑色固体 |
| B、红磷点燃后伸入氧气中产生大量白雾 |
| C、硫粉在氧气中燃烧产生明亮蓝紫色火焰 |
| D、常温下,向盛有过氧化氢溶液的试管加少量二氧化锰,产生大量气泡 |
反思是进步的阶梯,下列实验反思错误的是( )
| A、通过带火星的木条在氧气中复燃这个实验,我们可以反思得出检验氧气的方法 |
| B、通过碳、硫、磷、铁在空气中和氧气中燃烧的现象的不同,我们可以反思得出物质燃烧的剧烈程度和氧气的浓度有关 |
| C、通过对人体吸入和呼出的气体的探究实验,我们可以反思得出收集所有气体都可以用排水法 |
| D、通过空气成分测定实验,我们可以反思得出氮气不支持燃烧 |


