题目内容
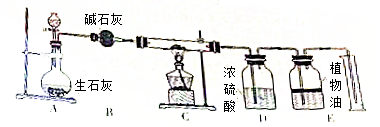
7.金属材料在生产、生活与科学研究中应用广泛.(1)钢铁是使用最多的金属材料,钢的硬度比纯铁的硬度大(填“大”或“小”);
(2)生活中使用的钢铁制品常会锈蚀,请写出一种防锈方法刷漆;
(3)西汉时期,我国首开“湿法炼铜”之先河,刘安所著的《淮南万毕术》中已有“曾青得铁则化为铜”的记载,请用一个化学方程式表示“湿法炼铜”的原理:Fe+CuSO4=FeSO4+Cu;
(4)某化学兴趣小组同学向含有Cu(NO3)2和AgNO3的溶液中,加入一定量的锌粉,充分反应后过滤,所得滤渣中只含一种金属,则滤液中一定含有的金属阳离子是锌离子和铜离子(填离子符号).
分析 (1)依据合金的一般性质分析解答;
(2)根据钢铁生锈的条件可以判断防止其生锈的方法;
(3)依据铁与硫酸铜反应的事实书写方程式;
(4)根据金属活动顺序表知:锌>铜>银,所以加入锌粉,首先锌粉和硝酸银溶液反应,置换出单质银,如果锌粉足量可以再继续和硝酸铜反应置换出铜解答.
解答 解:
(1)金属制成合金后合金的硬度一般要比纯金属硬度大,钢的硬度比纯铁的硬度大;
(2)铁在与水和氧气同时接触时容易生锈,要防锈可以使铁与水或氧气隔绝,可以在铁表面刷漆;
(3)由于铁的活动性比铜强所以铁可以置换出硫酸铜中的铜,其方程是为:Fe+CuSO4=FeSO4+Cu;
(4)金属活动性顺序可知,锌>铜>银,由题意可知,向含有AgNO3、Cu(NO3)2的混合液中加入一定量的锌粉,锌粉会首先置换硝酸银中的银,待硝酸银完全反应后继续与硝酸铜发生反应.
若滤渣中只含有一种金属,应该是银,所以滤液中一定含有的金属离子是锌离子和铜离子.
答案:
(1)大;
(2)刷漆;
(3)Fe+CuSO4=FeSO4+Cu;
(4)锌离子和铜离子.
点评 本题考查金属的性质,防止金属生锈的方法,金属活动性顺序的判断,化学方程式的书写等,基础性较强.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
2.推理是化学学习中常用的思维方法,下列推理中正确的是( )
| A. | 单质只含一种元素,所以含一种元素的物质一定是单质 | |
| B. | 中和反应生成盐和水,则生成盐和水的反应一定是中和反应 | |
| C. | 碱性溶液能使无色酚酞试液变红,能使无色酚酞试液变红的溶液一定是碱性溶液 | |
| D. | 离子是带电的原子或原子团,所以带电的微粒一定是离子 |
19. 溶液的应用非常广泛.
溶液的应用非常广泛.
K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下.
①图中能表示KNO3溶解度曲线的是甲(填“甲”或“乙”).
②曲线上M点的含义是t1℃时,甲和乙溶解度相等.
③20℃时,K2CO3饱和溶液中溶质与溶剂的质量比为79:250(结果用最简整数比表示).
④30℃时,向114g K2CO3固体中加入100g水,充分溶解后升温至40℃,该溶液中溶质的质量分数不变(填“变大”、“变小”或“不变”).
 溶液的应用非常广泛.
溶液的应用非常广泛.K2CO3和KNO3在不同温度时的溶解度及其溶解度曲线如下.
| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | K2CO3 | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |
②曲线上M点的含义是t1℃时,甲和乙溶解度相等.
③20℃时,K2CO3饱和溶液中溶质与溶剂的质量比为79:250(结果用最简整数比表示).
④30℃时,向114g K2CO3固体中加入100g水,充分溶解后升温至40℃,该溶液中溶质的质量分数不变(填“变大”、“变小”或“不变”).
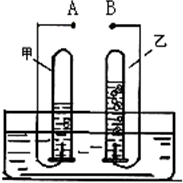 如图是电解水的简易装置图,回答下列问题.
如图是电解水的简易装置图,回答下列问题.