题目内容
4.如图是元素周期表的一部分,请回答相关问题:
(1)氟元素与氧元素位于第二周期的原因是原子核外有两个电子层,氟元素属于非金属(填“金属”或“非金属”)在化学反应中易得到(填“得到”或“失去”)电子.
(2)氧元素与硫元素化学性质相似的原因是最外层电子数相等;
(3)写出12号元素组成的单质和8号元素组成的单质反应的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
(4)同一周期(横行)的原子结构示意图具有的共同特点是电子层数相同(任写一点).
分析 (1)根据元素周期表的规律、元素的分类以及最外层电子数来分析;
(2)最外层电子数相同的元素化学性质相似;
(3)12号元素是镁,8号元素是氧,即镁燃烧生成氧化镁,再写出方程式即可;
(4)根据原子结构示意图的特点分析.
解答 解:(1)氟原子和氧原子的核外均有2个电子层,所以均位于第二周期;氟元素的汉字名称偏旁是“气”,所以属于非金属元素,氟原子的最外层有7个电子,在化学反应中易得电子;故填:原子核外有两个电子层;非金属;得到;
(2)从原子结构示意图的角度分析,氧元素与硫元素化学性质相似的原因是最外层电子数相等;故填:最外层电子数相等;
(3)12号元素是镁,8号元素是氧,即镁燃烧生成氧化镁,根据观察法配平即可,所以方程式是:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO,故填:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
(4)由原子结构示意图的特点可以看出,同一周期(横行)的原子结构示意图具有共同的特点是电子层数相同、最外层电子数由左向右依次增加等.故填:电子层数相同(答案合理即可).
点评 解答本题关键是熟悉元素周期表,知道化学方程式的写法,元素周期表的规律.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
15.氢氧化钙常用于改良酸性土壤,其俗称为( )
| A. | 生石灰 | B. | 大理石 | C. | 石灰石 | D. | 熟石灰 |
12.工业烟气脱硫就是将烟气中含有的二氧化硫除去.采用“双碱法”脱硫的工业流程如图.
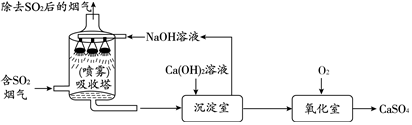
(1)吸收塔中,用NaOH溶液吸收SO2生成亚硫酸钠(Na2SO3)和水,NaOH溶液喷成雾状能充分吸收SO2的原因是增大吸收面积.
(2)沉淀室中发生的是复分解反应,化学方程式为Na2SO3+Ca(OH)2═CaSO3↓+2NaOH.
(3)氧化室中,化学反应的基本类型是化合反应.
(4)已知部分原料的价格如表所示.
上述工业流程中,处理相同量的SO2,双碱法所需的原料成本比用NaOH直接吸收更低,原因是实现了NaOH的循环利用,减少了NaOH的用量.

(1)吸收塔中,用NaOH溶液吸收SO2生成亚硫酸钠(Na2SO3)和水,NaOH溶液喷成雾状能充分吸收SO2的原因是增大吸收面积.
(2)沉淀室中发生的是复分解反应,化学方程式为Na2SO3+Ca(OH)2═CaSO3↓+2NaOH.
(3)氧化室中,化学反应的基本类型是化合反应.
(4)已知部分原料的价格如表所示.
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.90 |
5.用托盘天平称量10.2克(1克以下用游码)药品,如果称后发现误将砝码和称量物的置放颠倒了,则实际称得的药品质量为( )
| A. | 10.2克 | B. | 10克 | C. | 9.8克 | D. | 9克 |
2.蒸馒头、炸油条时常用到一种白色物质,它既能中和面粉发酵过程产生的酸,又能起发泡作用,这种白色物质是( )
| A. | NaOH | B. | Ca(OH)2 | C. | NaHCO3 | D. | NaCl |

 小明绘制的两种固体物质的溶解度曲线如图所示:
小明绘制的两种固体物质的溶解度曲线如图所示: