题目内容
8.“配制一定溶质质量分数的氯化钠溶液”是初中化学的基础实验之一,实验室用质量分数为15%的氯化钠溶液(密度为1.11g/cm3) 配制30g质量分数为5%的氯化钠溶液.(1)经计算,所取水的体积为20mL,所需15%的氯化钠溶液的体积为9mL.(水的密度为1g/cm3).
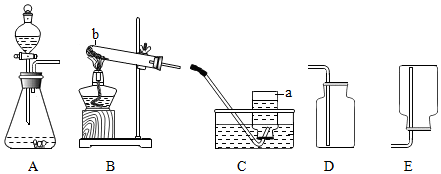
(2)量取上述体积的15%氯化钠溶液选用的仪器为A.(填选项)
A、10mL量筒 B、100mL烧杯 C、100mL量筒
(3)在实验室用质量分数为15%的氯化钠溶液配制质量分数为5%的氯化钠溶液的主要步骤有:计算、量取、稀释、装瓶并贴上标签.
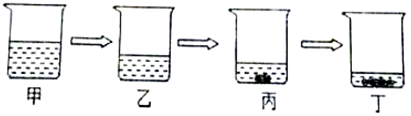
(4)实验室若用恒温蒸发的方法将15%的氯化钠溶液变成饱和溶液,其过程如图所示,与丙烧杯中溶液溶质质量分数一定相同的是丁烧杯中的溶液(填序号)
分析 (1)溶液稀释前后,溶质质量不变;
(2)选择量筒时,量程应该大于或等于量取的液体体积;
(3)在实验室用质量分数为15%的氯化钠溶液配制质量分数为5%的氯化钠溶液的主要步骤有:计算、量取、稀释、装瓶并贴上标签;
(4)饱和溶液溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%.
解答 解:(1)需要15%氯化钠溶液质量为:30g×5%÷15%=10g,
需要水的体积为:(30g-10g)÷1g/mL=20mL,
所需15%的氯化钠溶液的体积为:10g÷1.11g/cm3=9mL,
故填:20;9.
(2)量取上述体积的15%氯化钠溶液选用的仪器为10mL量筒.
故填:A.
(3)在实验室用质量分数为15%的氯化钠溶液配制质量分数为5%的氯化钠溶液的主要步骤有:计算、量取、稀释、装瓶并贴上标签.
故填:量取.
(4)丙和丁中烧杯中析出固体,因此丙和丁溶液都是饱和溶液,因此溶质质量分数相等.
故填:丁.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
16.化学兴趣小组的同学对实验氧气的制取进行了如图探究.
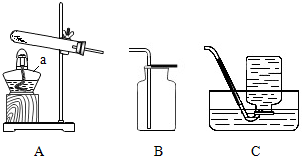
(1)仪器a的名称是酒精灯.
(2)实验室用高锰酸钾制取氧气的文字表达式为高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.用装置A、C制取氧气,收集完氧气时,应进行的操作是先将导管移出水面,再熄灭酒精灯.
(3)在老师指导下,同学们对一个化学反应可能有多种催化剂的问题进行了探究.
【提出猜想】除二气化锰(MnO2)外,氧化铜(CuO)、氧化铁(Fe2O3)也可以作氯酸钾(KClO3)
分解的催化剂.
【完成实验】按下表进行实验,并测定分解温度(分解温度越低,催化效果越好).
【分析与结论】对比实验①与④,可知氧化铁可加快氯酸钾分解的速率; 实验所用的三种
物质,催化效果最好的是二氧化锰.
【反思与拓展】若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质 不变; 同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证.

(1)仪器a的名称是酒精灯.
(2)实验室用高锰酸钾制取氧气的文字表达式为高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.用装置A、C制取氧气,收集完氧气时,应进行的操作是先将导管移出水面,再熄灭酒精灯.
(3)在老师指导下,同学们对一个化学反应可能有多种催化剂的问题进行了探究.
【提出猜想】除二气化锰(MnO2)外,氧化铜(CuO)、氧化铁(Fe2O3)也可以作氯酸钾(KClO3)
分解的催化剂.
【完成实验】按下表进行实验,并测定分解温度(分解温度越低,催化效果越好).
| 实验编号 | 实验药品 | 分解温度/℃ |
| ① | KClO3 | 580 |
| ② | KClO3、MnO2(质量比1:1) | 350 |
| ③ | KClO3、CuO(质量比1:1) | 370 |
| ④ | KClO3、Fe2O3(质量比1:1) | 390 |
物质,催化效果最好的是二氧化锰.
【反思与拓展】若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质 不变; 同种催化剂,颗粒大小可能影响催化效果,请设计实验方案进行验证.
| 实验步骤 | 实验现象 | 实验结论 |
| 小颗粒的分解温度为380℃, 大颗粒的分解温度为390℃ |
20.燃烧与缓慢氧化的共同点是( )
| A. | 都需要氧气参与 | B. | 反应都很剧烈 | C. | 都是氧化反应 | D. | 都要点燃 |
18.某科学教师安排两组同学做测定某NaOH和Na2CO3混合物中Na2CO3质量分数的实验:
(1)第一小组利用稀盐酸测定样品中Na2CO3的质量分数,用电子天平称量数据如下表:
①写出样品与盐酸发生化学反应的化学方程式:NaOH+HCl═NaCl+H2O,Na2CO3+2HCl═2NaCl+H2O+CO2↑.
②混合物中Na2CO3的质量分数为57%.
(2)第二组选用另一种方案测定样品(取m克)中Na2CO3的质量分数,其操作流程如下:

①A是BaCl2[Ba(OH)2、Ba(NO3)2](填化学式).该实验要求加入的A溶液必须过量,检查A溶液已经过量的方法是向过滤后所得澄清的滤液中滴加碳酸钠溶液,观察到有白色沉淀生成,说明所加入的氯化钡溶液过量
②计算混合物中Na2CO3的质量分数.(写出计算步骤.)
(1)第一小组利用稀盐酸测定样品中Na2CO3的质量分数,用电子天平称量数据如下表:
| 称 量 项 目 | 质量(克) |
| 所取样品 | 9.30 |
| 锥形瓶质量 | 41.20 |
| 锥形瓶+稀盐酸质量(过量) | 141.20 |
| 锥形瓶+稀盐酸质量+全部样品后,第一次称量的质量 | 148.50 |
| 锥形瓶+稀盐酸质量+全部样品后,第二次称量的质量 | 148.30 |
| 锥形瓶+稀盐酸质量+全部样品后,第三次称量的质量 | 148.30 |
②混合物中Na2CO3的质量分数为57%.
(2)第二组选用另一种方案测定样品(取m克)中Na2CO3的质量分数,其操作流程如下:

①A是BaCl2[Ba(OH)2、Ba(NO3)2](填化学式).该实验要求加入的A溶液必须过量,检查A溶液已经过量的方法是向过滤后所得澄清的滤液中滴加碳酸钠溶液,观察到有白色沉淀生成,说明所加入的氯化钡溶液过量
②计算混合物中Na2CO3的质量分数.(写出计算步骤.)