题目内容
4.实验室中常用过氧化氢溶液分解的方法制取氧气.若制取8瓶氧气(每个集气瓶的容积为250mL),至少需要分解多少克过氧化氢?(已知氧气的密度是1.429g/L).分析 根据题给的信息结合密度公式可以求算出氧气的质量,然后结合化学方程式可以求算出过氧化氢的质量.
解答 解:250mL×8=2000mL=2 L
制取氧气的质量为:1.429g/L×2L=2.858g
设需要过氧化氢的质量为X.
2H2O2═2 H2O+O2↑
68 32
X 2.858g
$\frac{68}{32}=\frac{X}{2.858g}$
X=$\frac{68×2.858g}{32}$=6.08g
答:至少需要分解6.08克过氧化氢.
点评 本题为根据化学方程式的基础计算,正确书写化学方程式、规范的计算步骤、准确的计算结果是解答时注意的关键.

练习册系列答案
相关题目
14.以下实验基本操作正确的是( )
| A. | 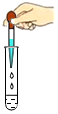 用滴管滴液 | B. |  加热液体 | C. | 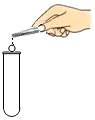 向试管加固体 | D. |  量取液体 |
15.无铅汽油一般是加入甲基叔丁基醚【CH3OC(CH3)3】作为高辛烷值组分.下列关于甲基叔丁基醚叙述错误的是( )
| A. | 甲基叔丁基醚属于化合物 | |
| B. | 甲基叔丁基醚的相对分子质量为88 | |
| C. | 甲基叔丁基醚中碳元素的质量分数约为68.2% | |
| D. | 一个甲基叔丁基醚分子是由5个碳原子、9个氢原子和1个氧原子构成的 |
12.粗盐的杂质主要是氯化镁(能溶于水),工业上常把粗盐粉碎后用饱和的食盐水浸泡,在过滤出食盐,对此,下列结论正确的( )
| A. | 浸洗前后,被浸洗的粗盐中氯化镁的含量基本不变 | |
| B. | 浸洗前后,饱和食盐水中氯化钠的质量基本不变 | |
| C. | 浸洗用的饱和食盐水可以无数次的使用下去 | |
| D. | 浸洗后,食盐水中氯化钠的质量增大 |
19.下列对宏观现象的微观解释,错误的是( )
| A. | 非吸烟者受到被动吸烟的危害,是因为分子在不断地运动 | |
| B. | 煤粉比煤块更容易燃烧,是因为煤粉与氧气的接触面积大 | |
| C. | 氧气性质活泼,是因为氧原子最外层电子数为6,极易失去电子 | |
| D. | 一氧化碳和二氧化碳具有不同的化学性质,是因为它们的分子组成不同 |
16.在KMnO4和K2MnO4中锰元素的化合价( )
| A. | 分别为+7、+6 | B. | 均为+6 | C. | 分别为+6、+7 | D. | 均为+7 |
13.对下列事实解释不正确的是( )
| 选项 | 事 实 | 解 释 |
| A | 一滴水中大约有1.67×1021个水分子 | 分子很小 |
| B | 敞口容器中的酒精逐渐减少 | 分子是不断运动的 |
| C | 体温计中的水银(汞)热胀冷缩 | 原子的体积热胀冷缩 |
| D | 炎热的夏天自行车车胎容易爆裂 | 夏天温度高,分子间隔变大 |
| A. | A | B. | B | C. | C | D. | D |
