题目内容
7.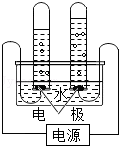 如图是电解水实验的简易装置图,回答下列有关问题:
如图是电解水实验的简易装置图,回答下列有关问题:(1)由实验现象可以确定:左面试管连接电池负极,若左面试管得到10mL气体,则右面试管得到5mL气体,可用带火星的木条检验右面气体的存在,电解水的文字表达式为水$\stackrel{通电}{→}$氢气+氧气,该反应的基本类型为分解反应.
(2)小丽同学将纯净的氢气点燃,观察到管口有淡蓝色火焰,将干燥的烧杯罩在火焰上方,烧杯内壁出现水雾.据此,她发现氢气的一个性质是能够燃烧;该反应的文字表达式为氢气+氧气$\stackrel{点燃}{→}$水,该反应的基本类型为化合反应,该性质决定了氢气是一种最理想的燃料.
分析 (1)根据正氧负氢、氢二氧一结合气体的性质和文字表达式的书写方法来分析;
(2)根据氢气的可燃性和燃烧的现象以及反应过程来分析.
解答 解:(1)侧试管内气体体积较大,是氢气,连接电源的负极;产生氢气与氧气的体积比为:2:1,故B试管内气体体积为5mL,氧气具有助燃性,可用带火星的木条来检验;水在通电的条件下分解为氢气和氧气,符合“一变多”的特征,属于分解反应;故填:负;5;带火星的木条;水$\stackrel{通电}{→}$氢气+氧气;分解反应;
(2)氢气燃烧发出淡蓝色火焰,将干燥的烧杯罩在火焰上方,烧杯内壁出现水雾,说明氢气具有可燃性,氢气与氧气在点燃的条件下生成水;符合“多变一”的特征,属于化合反应;因为氢气燃烧只生成水,对环境无污染,故为一种清洁高效的燃料.故填:淡蓝色;水雾;能够燃烧;氢气+氧气$\stackrel{点燃}{→}$水;化合反应.
点评 本题难度不大,掌握水的电解、化学变化的实质以及氢气的化学性质、氢能源的优缺点、文字表达式的书写等是正确解答本题的关键.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
16.人们在不同季节的制作过程中,一定发生了化学变化的是( )
| A. | 春天花朵掰成花瓣 | B. | 夏天西瓜榨成汁 | ||
| C. | 秋天粮食酿成美酒 | D. | 冬天冰砖凿成冰雕 |
12.催化剂在科研、医药生产和电子工业等前沿领域有着广泛应用.
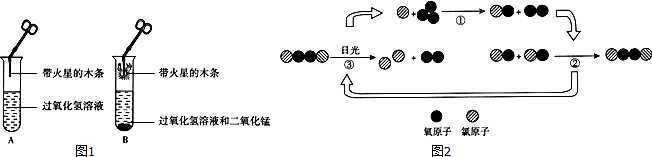
【实验1】验证二氧化锰是过氧化氢分解反应的催化剂
某同学设计如下实验:分别取5mL5%的过氧化氢溶液于两支试管中,向B中试管内加入少量二氧化锰(如图1所示).A中带火星的木条不复燃,B中带火星的木条复燃.
A中木条不复燃的原因是氧气的浓度不够或没有氧气产生,B中反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
有同学认为上述实验方案不足以证明二氧化锰是该反应的催化剂,理由是不能证明二氧化锰在反应前后的质量和化学性质没有改变.
【实验2】为探究二氧化锰对氯酸钾分解的催化作用.在相同条件下,同学们按下表进行实验,并记录相关数据.(其他影响实验的因素均相同)
①表中a的数值应是2.0;
②表中的待测数据指D(填字母序号).
A.氧气的质量 B.反应后固体的质量
C.氧气的体积 D.单位时间内产生氧气的体积
③设计“实验1”的目的是对比.
【拓展】
(1)同学们继续探究二氧化锰是否参与了氯酸钾的分解反应.
氯酸钾和二氧化锰混合加热的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KC1+302↑.已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空.
(I)2KC103+2Mn02$\frac{\underline{\;\;△\;\;}}{\;}$2KMn04+Cl2↑+02↑;
(Ⅱ)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑(用化学方程式表示);
(Ⅲ)K2Mn04+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+Mn02+02↑.
通过以上分析,同学们得出结论:二氧化锰参与了氯酸钾的分解反应.
(2)氟利昂释放出的氯原子参与了臭氧层的破坏,其他微观示意图如图2,综合图中①②③的反应过程,写出臭氧层被破坏的化学方程式:2O3$\frac{\underline{\;\;\;CL\;\;\;}}{日光}$3O2.

【实验1】验证二氧化锰是过氧化氢分解反应的催化剂
某同学设计如下实验:分别取5mL5%的过氧化氢溶液于两支试管中,向B中试管内加入少量二氧化锰(如图1所示).A中带火星的木条不复燃,B中带火星的木条复燃.
A中木条不复燃的原因是氧气的浓度不够或没有氧气产生,B中反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
有同学认为上述实验方案不足以证明二氧化锰是该反应的催化剂,理由是不能证明二氧化锰在反应前后的质量和化学性质没有改变.
【实验2】为探究二氧化锰对氯酸钾分解的催化作用.在相同条件下,同学们按下表进行实验,并记录相关数据.(其他影响实验的因素均相同)
| 编号 | KC103 质量/g | 其他物质质量/g | 待测数据 |
| 实验1 | 2.0 | / | |
| 实验2 | a | Mn02 0.5 |
②表中的待测数据指D(填字母序号).
A.氧气的质量 B.反应后固体的质量
C.氧气的体积 D.单位时间内产生氧气的体积
③设计“实验1”的目的是对比.
【拓展】
(1)同学们继续探究二氧化锰是否参与了氯酸钾的分解反应.
氯酸钾和二氧化锰混合加热的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KC1+302↑.已知氯酸钾与二氧化锰混合加热时连续发生如下反应,试分析后按要求填空.
(I)2KC103+2Mn02$\frac{\underline{\;\;△\;\;}}{\;}$2KMn04+Cl2↑+02↑;
(Ⅱ)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑(用化学方程式表示);
(Ⅲ)K2Mn04+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+Mn02+02↑.
通过以上分析,同学们得出结论:二氧化锰参与了氯酸钾的分解反应.
(2)氟利昂释放出的氯原子参与了臭氧层的破坏,其他微观示意图如图2,综合图中①②③的反应过程,写出臭氧层被破坏的化学方程式:2O3$\frac{\underline{\;\;\;CL\;\;\;}}{日光}$3O2.
19.实验室区分下列物质的实验方法或操作完全错误的是( )
| A | B | C | D | |
| 酒精和水 | 空气和二氧化碳 | 汞和硫 | 木炭粉和二氧化锰 | |
| 方法一 | 品尝 | 带火星木条 | 看状态 | 看颜色 |
| 方法二 | 点燃 | 燃着的木条 | 看颜色 | 是否溶于水 |
| A. | A | B. | B | C. | C | D. | D |
16.生活中处处充满化学,下列广告语中叙述不正确的是( )
| A. | 本产品不含任何化学物质 | |
| B. | 本食品袋内充有氮气,有更长的保质期 | |
| C. | 空气是人类宝贵的自然财富 | |
| D. | 请爱护水资源,合理使用水资源,否则人类见到的最后一滴水可能是他的眼泪 |
17.下列实验装置设计或实验操作正确的是( )
| A. | 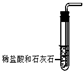 制取CO2 | B. | 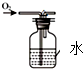 监控气体流速 | C. |  检查装置气密性 | D. |  验证O2的性质 |
