题目内容
15.已知CaO+H2O=Ca(OH)2,取CaO和Ca(OH)2共10克,含Ca%40%,加入足量水反应后,再通入足量CO2,生成沉淀多少克?分析 根据氧化钙和水反应会生成氢氧化钙,氢氧化钙和二氧化碳反应会生成碳酸钙沉淀,结合题中的数据进行计算.
解答 解:CaO和Ca(OH)2共10克,含Ca%40%,所以钙元素的质量是:10g×40%=4g,钙元素会转化成碳酸钙,
设生成碳酸钙沉淀质量为x,
Ca------CaCO3
40 100
4g x
$\frac{40}{4g}$=$\frac{100}{x}$
x=10g
答:生成碳酸钙质量为10g.
点评 本题主要考查了利用元素守恒的化学计算,难度不大,需要注意解题的规范性.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
5.下列做法存在安全隐患的是( )
| A. | 炒菜时油锅着火,立刻盖上锅盖 | |
| B. | 维修沼气池前,先做灯火实验 | |
| C. | 室内发生火灾,应打开所有门窗通风 | |
| D. | 发现液化气泄漏,关闭阀门并开窗通风 |
10.测大理石纯度,取400克稀盐酸等分为4等份
M=6.6克,哪几次大理石过量第四次,大理石纯度50%,稀盐酸纯度11.6%,完成.
| 第一份 | 第二份 | 第三份 | 第四份 |
| 大理石 10克 | 20克 | 30克 | 40克 |
| CO2 2.2克 | 4.4克 | M | 7克 |
7. 中国“控烟”任重道远,需要我们向那些不守法的烟民大声说出:“被吸烟,我不干!”造成非吸烟者在公共场所吸食“二手烟”的主要原因是( )
中国“控烟”任重道远,需要我们向那些不守法的烟民大声说出:“被吸烟,我不干!”造成非吸烟者在公共场所吸食“二手烟”的主要原因是( )
 中国“控烟”任重道远,需要我们向那些不守法的烟民大声说出:“被吸烟,我不干!”造成非吸烟者在公共场所吸食“二手烟”的主要原因是( )
中国“控烟”任重道远,需要我们向那些不守法的烟民大声说出:“被吸烟,我不干!”造成非吸烟者在公共场所吸食“二手烟”的主要原因是( )| A. | 分子很小 | B. | 分子在不断运动 | C. | 分子之间有间隙 | D. | 分子由原子构成 |
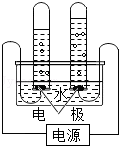 如图是电解水实验的简易装置图,回答下列有关问题:
如图是电解水实验的简易装置图,回答下列有关问题: