题目内容
16.下列变化中前者是物理变化,后者是化学变化的是( )| A. | 铁矿石炼铁,电解水制氧气 | B. | 干冰变为CO2气体,用盐酸除锈 | ||
| C. | 无水硫酸铜遇水变蓝,轮胎爆炸 | D. | 磷在空气中燃烧,用液态空气制O2 |
分析 判断一个变化是物理变化还是化学变化,要依据在变化过程中有没有生成其他物质,生成其他物质的是化学变化,没有生成其他物质的是物理变化.
解答 解:A、铁矿石炼铁是利用还原剂与铁的化合物反应生成铁,属于化学变化;电解水制氧气的过程中有新物质氧气生成,属于化学变化;
B、干冰变为CO2气体的过程没有新物质生成,属于物理变化;用盐酸除锈的过程中有新物质生成,属于化学变化;
C、无水硫酸铜遇水变蓝的过程中有新物质生成,属于化学变化;汽车内胎爆炸是由于压强大造成的,没有新物质生成,属于物理变化;
D、磷在空气中燃烧的过程中有新物质生成,属于化学变化;用液态空气制O2的过程中没有新物质生成,属于物理变化;
故选B.
点评 搞清楚物理变化和化学变化的本质区别是解答本类习题的关键.判断的标准是看在变化中有没有生成其他物质.一般地,物理变化有物质的固、液、气三态变化和物质形状的变化.

练习册系列答案
相关题目
6.工业上以高纯度的二氧化锰为原料制备高锰酸钾的主要流程如下:

已知相关物质的溶解度(20℃)如下表:
(1)KMnO4中锰元素的化合价为+7.
(2)操作I的名称是过滤.“干燥”过程中温度不宜过高的原因是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑(用化学方程式表示).
(3)“通CO2酸化”,反应的化学方程式为:3K2 MNO4+2CO2═2KmnO4+MnO2↓+2K2 CO3
著用稀H2SO4酸化,反应的化学方程式为:3K2 MNO4+2H2 SO4═2KMnO4+MnO2↓+2K2SO4+2H2O
工业上不采用稀H2SO4酸化的原因是相同条件下,硫酸钾和高锰酸钾的溶解度都比较小,无法采用浓缩结晶的方法加以分离.
(4)电解法也可以实现由K2MnO4向KMnO4的转化,反应的化学方程式为:3K2 MNO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2KMnO4+2KOH+H2↑,与“通CO2酸化”相比,其优点是生成的氢氧化钾可以循环使用.

已知相关物质的溶解度(20℃)如下表:
| 物质 | K2CO3 | K2SO4 | KMnO4 |
| 溶解度/g | 111 | 11.1 | 6.34 |
(2)操作I的名称是过滤.“干燥”过程中温度不宜过高的原因是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑(用化学方程式表示).
(3)“通CO2酸化”,反应的化学方程式为:3K2 MNO4+2CO2═2KmnO4+MnO2↓+2K2 CO3
著用稀H2SO4酸化,反应的化学方程式为:3K2 MNO4+2H2 SO4═2KMnO4+MnO2↓+2K2SO4+2H2O
工业上不采用稀H2SO4酸化的原因是相同条件下,硫酸钾和高锰酸钾的溶解度都比较小,无法采用浓缩结晶的方法加以分离.
(4)电解法也可以实现由K2MnO4向KMnO4的转化,反应的化学方程式为:3K2 MNO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2KMnO4+2KOH+H2↑,与“通CO2酸化”相比,其优点是生成的氢氧化钾可以循环使用.
7.下列属于合成材料的是( )
| A. | 不锈钢 | B. | 蚕丝 | C. | 腈纶 | D. | 乙醇 |
4.金属镍及其化合物能发生下列反应:①Ni+2HCl=NiCl2+H2↑;②NiO+2HCl=NiCl2+H2O;③NiO2+4HCl=NiCl2+Cl2↑+2H20;分析化学方程式可知,下列说法中错误的是( )
| A. | 镍能从硫酸铜溶液中置换出铜 | |
| B. | 反应①属于复置换反应 | |
| C. | 反应③中Ni的化合价由+4价变为+2价 | |
| D. | 上述3个反应中涉及2种单质 |
1.实验室用H2还原m克CuO,反应进行一会儿后,停止加热,冷却后称量,余下的质量为n克,实验中共用去氢气的质量为W克,反应后还剩CuO的质量为( )
| A. | (4m-5n)克 | B. | (5n-4m)克 | C. | (5m-5n) 克 | D. | (m-n)克 |
5.在硝酸铜、硝酸锌、硝酸银三种物质的混合溶液里,加入过量的铁粉,充分反应后过滤,滤液中存在的金属离子是( )
| A. | Fe2+、Zn2+ | B. | Cu2+、Zn2+ | C. | Fe3+、Zn2+ | D. | Cu2+、Ag+ |
6.下列通过实验得出的结论,其中不合理的是( )
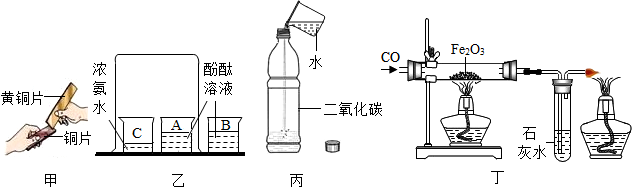

| A. | 甲实验中黄铜片能在铜片上刻画出痕迹可以说明黄铜的硬度比铜大 | |
| B. | 乙实验既可以说明分子在不停地运动着,又可以说明氨水显碱性 | |
| C. | 丙实验既可以说明二氧化碳易溶于水,又可以说明二氧化碳具有酸性 | |
| D. | 丁实验既可以说明一氧化碳具有还原性,又可以说明一氧化碳具有可燃性 |