题目内容
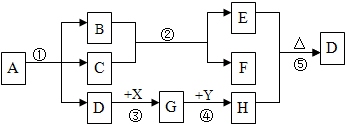
6.工业上以高纯度的二氧化锰为原料制备高锰酸钾的主要流程如下:
已知相关物质的溶解度(20℃)如下表:
| 物质 | K2CO3 | K2SO4 | KMnO4 |
| 溶解度/g | 111 | 11.1 | 6.34 |
(2)操作I的名称是过滤.“干燥”过程中温度不宜过高的原因是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑(用化学方程式表示).
(3)“通CO2酸化”,反应的化学方程式为:3K2 MNO4+2CO2═2KmnO4+MnO2↓+2K2 CO3
著用稀H2SO4酸化,反应的化学方程式为:3K2 MNO4+2H2 SO4═2KMnO4+MnO2↓+2K2SO4+2H2O
工业上不采用稀H2SO4酸化的原因是相同条件下,硫酸钾和高锰酸钾的溶解度都比较小,无法采用浓缩结晶的方法加以分离.
(4)电解法也可以实现由K2MnO4向KMnO4的转化,反应的化学方程式为:3K2 MNO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2KMnO4+2KOH+H2↑,与“通CO2酸化”相比,其优点是生成的氢氧化钾可以循环使用.
分析 (1)根据在化合物中正负化合价代数和为零,结合化学式进行解答本题;
(2)根据分离混合物的方法以及高锰酸钾受热易分解来分析;
(3)根据物质的溶解度来分析;
(4)根据反应的产物来分析.
解答 解:(1)钾元素显+1价,氧元素显-2价,设锰元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(-2)×4=0,则x=+7;
(2)操作Ⅰ是分离固体与液体,是过滤操作;干燥高锰酸钾粗晶体的过程中温度不宜过高的原因是高锰酸钾在加热的条件下会分解为锰酸钾、二氧化锰和氧气,反应方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)由溶解度表可知,在相同条件下,碳酸钾的溶解度远远大于高锰酸钾的溶解度,所以可采用浓缩结晶的方法加以分离;而相同条件下,硫酸钾和高锰酸钾的溶解度都比较小,无法采用浓缩结晶的方法加以分离;
(4)电解法的产物之一是氢氧化钾,可以在工艺流程中用作反应的原料;
故答案为:(1)+7;
(2)过滤;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)相同条件下,硫酸钾和高锰酸钾的溶解度都比较小,无法采用浓缩结晶的方法加以分离;
(4)生成的氢氧化钾可以循环使用.
点评 本题考查学生对工艺流程的理解、阅读获取信息能力、工艺条件的控制等,难度中等,是对所学知识的综合运用与能力的考查,需要学生具备扎实的基础知识与综合运用知识、信息进行解决问题的能力.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
3.下列说法不正确的是( )
| A. | 纸是中国古代四大发明之一,属于天然纤维 | |
| B. | 中空塑件属于天然材料,不会产生任何污染 | |
| C. | 奥林匹克圣火的燃烧是化学变化,一切燃烧都是化学变化 | |
| D. | 丙烷燃烧属于氧化反应 |
16.下列变化中前者是物理变化,后者是化学变化的是( )
| A. | 铁矿石炼铁,电解水制氧气 | B. | 干冰变为CO2气体,用盐酸除锈 | ||
| C. | 无水硫酸铜遇水变蓝,轮胎爆炸 | D. | 磷在空气中燃烧,用液态空气制O2 |
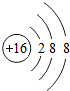 ;
;