题目内容
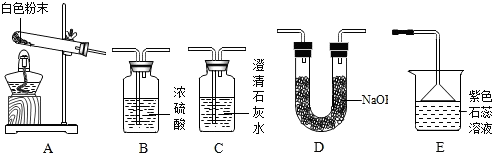
一包白色粉末A由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的三种混合而成.为探究其组成,进行以下实验: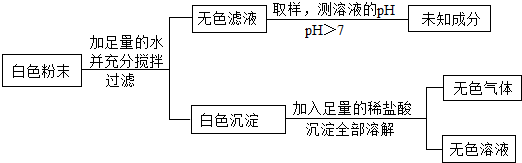
分析实验过程,回答:
①白色粉末A中一定有 ,一定没有 ;可能含有的物质是 生成无色气体E的化学方程式是 .
②对可能含有的物质,通过如下实验进一步确认:

分析实验过程,回答:
①白色粉末A中一定有
②对可能含有的物质,通过如下实验进一步确认:
| 实验操作 | 实验现象 | 实验结论 |
| 取未知成分溶液D少许,加入 |
考点:物质的鉴别、推断,溶液的酸碱性与pH值的关系,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:混合物组成的推断题
分析:根据硫酸铜溶于水得到蓝色溶液,而本题中得到是无色的溶液,所以在混合物中一定不含硫酸铜;同时能形成白色沉淀的为碳酸钙,而白色沉淀能全部溶于稀盐酸,硫酸钠和氯化钡反应生成的硫酸钡不溶于稀盐酸,所以该沉淀为碳酸钙;已知无色溶液PH>7,为氢氧化钠;可以据此分析判断并解答该题.
解答:解:①把白色粉末溶解后得无色溶液,可知一定没有硫酸铜,因为硫酸铜溶于水会使溶液变蓝;实验中的白色固体可能是碳酸钙,也可能是氯化钡和硫酸钠反应产生的硫酸钡沉淀,而框图中的白色沉淀全部溶于稀盐酸中,并产生无色气体,说明这种白色沉淀是碳酸钙;与稀盐酸反应产生气泡的化学方程式为 CaCO3+2HCl═CaCl2+H2O+CO2↑;
②由于该白色粉末是三种混合而成,由实验可以分析出硫酸钠和氯化钡只能存在一种,要验证氯化钡或硫酸钠的存在,可以通过验证钡离子或硫酸根离子的存在,因此可以滴加硫酸或氯化钡观察是否产生沉淀进行验证.
故答案为:①NaOH、CaCO3,CuSO4;氯化钡和硫酸钠中的一种;CaCO3+2HCl═CaCl2+H2O+CO2↑;
②
(答案合理即可).
②由于该白色粉末是三种混合而成,由实验可以分析出硫酸钠和氯化钡只能存在一种,要验证氯化钡或硫酸钠的存在,可以通过验证钡离子或硫酸根离子的存在,因此可以滴加硫酸或氯化钡观察是否产生沉淀进行验证.
故答案为:①NaOH、CaCO3,CuSO4;氯化钡和硫酸钠中的一种;CaCO3+2HCl═CaCl2+H2O+CO2↑;
②
| 实验操作 | 实验现象 | 实验结论 |
| 取未知成分溶液D少许,加入 氯化钡溶液, | 白色沉淀(或没有沉淀) | 有硫酸钠 (或氯化钡). |
点评:本题属于框图式推断题,在给定的物质范围和实验现象,来推出混合物中一定存在、一定不存在和可能存在的是什么物质;解答时以框图信息为序,寻找并抓住“题眼”,逐步分析“筛选”最终得出答案即可.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质的化学式书写正确的是( )
| A、氧化镁MgO2 |
| B、氧化铝AL2O3 |
| C、碳酸钠NaCO3 |
| D、二氧化氮NO2 |
下列物质中,属于纯净物的是( )
| A、食用醋 | B、干冰 |
| C、清洁空气 | D、加碘食盐 |
下列各组物质对应的鉴别方法正确的是( )
| A、黄金和黄铜--滴加稀盐酸 |
| B、双氧水和蒸馏水--观察颜色 |
| C、硬水和软水--观察是否澄清 |
| D、生理盐水和葡萄糖注射液--加紫色石蕊溶液 |
每年5月31日为世界无烟日,从今年1月9日起,我国承诺实现公共场所全面禁烟.吸烟有害健康,烟气中的一种有毒气体是( )
| A、O2 |
| B、N2 |
| C、CO |
| D、CO2 |
海洋是重要的资源,利用海水可以得到许多产品.①海水“晒盐”;②海水“制碱”;③海水“淡化”;④从海水中提取镁.其中主要利用化学变化的是( )
| A、全部 | B、①②④ |
| C、只有② | D、只有②④ |
 如图是某保健品标签的部分内容,请仔细阅读后回答下列问题
如图是某保健品标签的部分内容,请仔细阅读后回答下列问题