题目内容
化学小组同学发现在面包制作过程中加入了一些白色粉末,使面包变得松软.同学们对白色粉末的成分进行探究.
【查阅资料】
①经调查,市场上有以下3种主要产品.
②氨气(NH3)是一种有刺激性气味的气体,极易溶于水,其水溶液显碱性.
③2NaHCO3
Na2CO3+H2O+CO2↑;2NH3+H2SO4=(NH4)2SO4
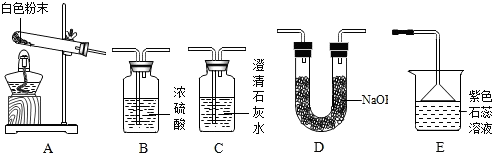
【实验准备】同学们选用下列实验装置,经组合进行实验:
【实验记录】
【实验分析】
根据上述实验,甲同学认为该粉末的主要成分为食臭粉.写出食臭粉加热反应的化学方程式
;
乙同学认为上述实验不能确定该粉末为食臭粉.为进一步确认其组成及含量,同学们设计了如表定量实验:
(1)实验3中装置B的作用是 ;
(2)实验3中测得装置D增重a g,a的范围是 ;
(3)若测得a为13.2,该碱性膨松剂中NaHCO3与NH4HCO3的质量比为 (结果用最简整数比表示).

【查阅资料】
①经调查,市场上有以下3种主要产品.
| 商品名称 | 小苏打 | 食臭粉 | 混合碱性膨松剂 |
| 主要成分 | 碳酸氢钠 | 碳酸氢铵 | 碳酸氢钠和碳酸氢铵 |
③2NaHCO3
| ||
【实验准备】同学们选用下列实验装置,经组合进行实验:
【实验记录】
| 实验序号 | 实验装置 | 实验现象 | 实验结论及分析 |
| 实验1 | 选用A、B、C | C中 | 有CO2生成 |
| 实验2 | 选用A、 | E中紫色石蕊溶液变成 | 有NH3生成 |
根据上述实验,甲同学认为该粉末的主要成分为食臭粉.写出食臭粉加热反应的化学方程式
乙同学认为上述实验不能确定该粉末为食臭粉.为进一步确认其组成及含量,同学们设计了如表定量实验:
| 实验序号 | 实验目的 | 实验装置 | 数据记录 | 实验结论 |
| 实验3 | 测定生成CO2的质量 | 选用A、B、D | 装置D增重a g | 该粉末为“混合碱性膨松剂” |
| 实验4 | 测定生成NH3的质量 | 选用A、B、D | 装置B增重1.7g |
(2)实验3中测得装置D增重a g,a的范围是
(3)若测得a为13.2,该碱性膨松剂中NaHCO3与NH4HCO3的质量比为
考点:实验探究物质的组成成分以及含量,常见气体的检验与除杂方法,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:由题目的信息可知:
【实验记录】选用A,B,C,C中澄清石灰水变浑浊,是二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水;选用A,D,E,D是吸收二氧化碳和水蒸气的,E是检验氨气的,氨气溶于水是氨水,氨水能使紫色石蕊试液变蓝色;
【实验分析】根据食臭粉加热反应的反应物、生成物、反应条件,书写化学方程式;
实验3中装置B的作用是:除尽水蒸气和氨气,装置D增重的质量是二氧化碳的质量;如果装置B增重1.7g,因为碳酸氢铵受热分解生成一份氨气和一份二氧化碳,那么生成二氧化碳的质量是4.4g,又因为碳酸氢钠分解也生成二氧化碳,因此a大于4.4g;若测得a为92.4g,那么碳酸氢钠分解生成的二氧化碳的质量=92.4g-4.4g=88g,根据88g二氧化碳的质量求碳酸氢钠的质量,然后求NaHCO3与NH4HCO3的质量比.
【实验记录】选用A,B,C,C中澄清石灰水变浑浊,是二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水;选用A,D,E,D是吸收二氧化碳和水蒸气的,E是检验氨气的,氨气溶于水是氨水,氨水能使紫色石蕊试液变蓝色;
【实验分析】根据食臭粉加热反应的反应物、生成物、反应条件,书写化学方程式;
实验3中装置B的作用是:除尽水蒸气和氨气,装置D增重的质量是二氧化碳的质量;如果装置B增重1.7g,因为碳酸氢铵受热分解生成一份氨气和一份二氧化碳,那么生成二氧化碳的质量是4.4g,又因为碳酸氢钠分解也生成二氧化碳,因此a大于4.4g;若测得a为92.4g,那么碳酸氢钠分解生成的二氧化碳的质量=92.4g-4.4g=88g,根据88g二氧化碳的质量求碳酸氢钠的质量,然后求NaHCO3与NH4HCO3的质量比.
解答:解:
【实验记录】选用A,B,C,C中澄清石灰水变浑浊,是二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水;选用A,D,E,D是吸收二氧化碳和水蒸气的,E是检验氨气的,氨气溶于水是氨水,氨水能使紫色石蕊试液变蓝色,故答案为:实验1:澄清石灰水变浑浊;实验2:D;蓝;
【实验分析】
根据实验中的现象,则食臭粉加热反应的化学方程式为NH4HCO3
NH3↑+H2O+CO2↑;
(1)实验3中装置B的作用是:除尽水蒸气和氨气,装置D增重的质量是二氧化碳的质量;
(2)如果装置B增重1.7g,因为碳酸氢铵受热分解生成一份氨气和一份二氧化碳,那么生成二氧化碳的质量是4.4g,又因为碳酸氢钠分解也生成二氧化碳,因此a大于4.4g;
(3)若测得a为92.4g,那么碳酸氢钠分解生成的二氧化碳的质量=92.4g-4.4g=88g,根据88g二氧化碳的质量求碳酸氢钠的质量,然后求NaHCO3与NH4HCO3的质量比;设生成88g二氧化碳需要碳酸氢钠的质量为x
2NaHCO3
Na2CO3+H2O+CO2↑
168 44
x 88g
则
=
,解得 x=336g,
因此NaHCO3与NH4HCO3的质量比=336g:7.9g=3360:79.
故答案为:
【实验记录】
【实验分析】
NH4HCO3
NH3↑+H2O+CO2↑;
(1)除尽水蒸气和氨气;
(2)>4.4;
(3)3360:79
【实验记录】选用A,B,C,C中澄清石灰水变浑浊,是二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水;选用A,D,E,D是吸收二氧化碳和水蒸气的,E是检验氨气的,氨气溶于水是氨水,氨水能使紫色石蕊试液变蓝色,故答案为:实验1:澄清石灰水变浑浊;实验2:D;蓝;
【实验分析】
根据实验中的现象,则食臭粉加热反应的化学方程式为NH4HCO3
| ||
(1)实验3中装置B的作用是:除尽水蒸气和氨气,装置D增重的质量是二氧化碳的质量;
(2)如果装置B增重1.7g,因为碳酸氢铵受热分解生成一份氨气和一份二氧化碳,那么生成二氧化碳的质量是4.4g,又因为碳酸氢钠分解也生成二氧化碳,因此a大于4.4g;
(3)若测得a为92.4g,那么碳酸氢钠分解生成的二氧化碳的质量=92.4g-4.4g=88g,根据88g二氧化碳的质量求碳酸氢钠的质量,然后求NaHCO3与NH4HCO3的质量比;设生成88g二氧化碳需要碳酸氢钠的质量为x
2NaHCO3
| ||
168 44
x 88g
则
| 168 |
| 44 |
| x |
| 88g |
因此NaHCO3与NH4HCO3的质量比=336g:7.9g=3360:79.
故答案为:
【实验记录】
| 实验序号 | 实验装置 | 实验现象 | 实验结论及分析 |
| 实验1 | 澄清石灰水变浑浊 | ||
| 实验2 | D | 蓝 |
NH4HCO3
| ||
(1)除尽水蒸气和氨气;
(2)>4.4;
(3)3360:79
点评:本考点既考查了实验步骤的设计,又考查了化学方程式的书写,还对实验进行了评价,综合性比较强.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.

练习册系列答案
相关题目
正确读写化学符号是学好化学的基础,下列读法或写法正确的是( )
| A、3H-3个氢分子 |
| B、氧氧化铁-Fe( OH) |
| C、AlCl2-氯化铝 |
| D、2Ba2+-2个钡离子 |
下列四组物质中,依次属于单质、氧化物、盐的是( )
| A、氦气、氧化铜、铁强化食用盐 |
| B、水、二氧化硫、氯酸钾 |
| C、氧气、氧化铁、硫酸铜 |
| D、水银、氧化镁、氨水 |
下列家庭实验中不涉及化学变化的是( )
| A、用少量食醋除去水壶中的水垢 |
| B、用糯米、酒曲和水制甜酒酿 |
| C、光合作用 |
| D、用木炭除去冰箱中的异味 |
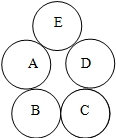 A、B、C、D、E分别是氧化铁、铁、氧气、单质碳、稀硫酸中的一种物质. 用五个圆表示五种物质,用两圆相切表示两种物质可以发生化学反应. 请回答下列问题:
A、B、C、D、E分别是氧化铁、铁、氧气、单质碳、稀硫酸中的一种物质. 用五个圆表示五种物质,用两圆相切表示两种物质可以发生化学反应. 请回答下列问题: