题目内容
4.1946年2月14日第一台计算机问世以来,仅用60年的时间已经走进我们的生活.(1)计算机和打印机所用导线的内部材料及电源插头等都是金属铜,这是利用了铜具有①导电性,铁制文件柜表面要喷漆,其目的是②防锈、美观;
(2)打印机在工作过程中实现的能量转化是电能转化为机械能;
(3)计算机内部印刷线路板的线路走向,是采用氯化铁溶液和金属铜反应完成的,生成物是两种正二价的金属氯化物,其反应的化学方程式为①2FeCl3+Cu═2FeCl2+CuCl2;反应过程中铁元素的化合价变化为②+3价变为+2价.
分析 (1)①根据导线与电源的插头的作用考虑;②根据铁制的文件柜表面要喷漆的作用考虑;
(2)根据打印机的工作原理考虑;
(3)根据方程式的写法和题干中提供的信息考虑.
解答 解:(1)①导线与电源的插头必须能够导电,所以是利用了铜的导电性;②铁制的文件柜表面喷漆隔绝了空气,使铁与空气和水不接触,所以防止铁柜生锈,同时能美观;
(2)打印机在工作过程中需要通电,所以是电能转化为机械能再打印在纸上;
(3)由题意可知,反应物是铁和氯化铁,生成物是氯化铜和氯化亚铁,反应的方程式是:Cu+2FeCl3═CuCl2+2FeCl2;在反应物氯化铁中铁是+3价,在生成物是两种正二价的金属氯化物,铁为+2价,所以反应过程中铁元素的化合价变化为由+3价变为+2价.
故答为:(1)①导电,②防锈、美观;(2)电能转化为机械能;(3)①2FeCl3+Cu═2FeCl2+CuCl2;②+3价变为+2价.
点评 解答本题关键是要知道物质的用途反映物质的性质,防止生锈的方法,知道方程式的书写方法.

练习册系列答案
相关题目
14.山茶油是一种绿色保健食品,其主要成分是柠檬醛,现从山茶油中提取7.6g柠檬醛,使其在氧气中完全燃烧,生成2.2g二氧化碳和7.2克水,则柠檬醛中( )
| A. | 一定含碳、氢、氧元素 | |
| B. | 只含碳、氢元素 | |
| C. | 一定含碳、氢元素,可能含有氧元素 | |
| D. | 碳、氢、氧元素的原子个数比为10:8:1 |
12.实验室常用的干燥剂“碱石灰”是CaO和NaOH固体的混合物.同学们为确认一瓶久置的“碱石灰”样品的成分,进行如下实验探究.
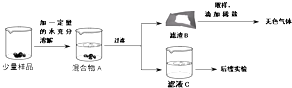
滤渣B中一定含有CaCO3,产生该物质的化学方程式可能是Ca(OH)2+Na2CO3=CaCO3↓+2NaOH滤液C成分的探究.
【猜想】滤液C中的溶质可能为①NaOH;②Na2CO3;③NaOH和Na2CO3;④NaOH和Ca(OH)2
【设计方案并进行实验】甲、乙同学分别设计如下方案并进行探究:
甲同学:取滤液C少许放入试管中,滴加足量的稀盐酸,产生大量无色气体,则滤液C中的溶质是Na2CO3.
乙同学:取滤液C少许放入试管中,滴加一定量的无色酚酞,液体变成红色,则滤液C中的溶质一定含有NaOH.
【反思与评价】丙同学认真分析上述两位同学的实验,认为他们的结论均有不足之处,请说出丙认为甲、乙同学不足之处的理由甲同学:加入足量盐酸,产生大量气体,可能有氢氧化钠被消耗后与碳酸钠溶液反应;
乙同学:实验中加无色酚酞溶液,变红则滤液中还可能有碳酸钠,碳酸钠溶液也能使酚酞变红;为进一步确认猜想③正确,请你帮助他设计实验进行验证.
实验过程中,同学们还发现向样品中加入一定量水溶解时放出大量的热并综合对滤液和滤渣成分的探究,下列对样品成分的分析正确的是②③(填序号).①样品中一定含NaOH ②样品中一定含Na2CO3
③样品中含NaOH、CaO中的一种或两种.

滤渣B中一定含有CaCO3,产生该物质的化学方程式可能是Ca(OH)2+Na2CO3=CaCO3↓+2NaOH滤液C成分的探究.
【猜想】滤液C中的溶质可能为①NaOH;②Na2CO3;③NaOH和Na2CO3;④NaOH和Ca(OH)2
【设计方案并进行实验】甲、乙同学分别设计如下方案并进行探究:
甲同学:取滤液C少许放入试管中,滴加足量的稀盐酸,产生大量无色气体,则滤液C中的溶质是Na2CO3.
乙同学:取滤液C少许放入试管中,滴加一定量的无色酚酞,液体变成红色,则滤液C中的溶质一定含有NaOH.
【反思与评价】丙同学认真分析上述两位同学的实验,认为他们的结论均有不足之处,请说出丙认为甲、乙同学不足之处的理由甲同学:加入足量盐酸,产生大量气体,可能有氢氧化钠被消耗后与碳酸钠溶液反应;
乙同学:实验中加无色酚酞溶液,变红则滤液中还可能有碳酸钠,碳酸钠溶液也能使酚酞变红;为进一步确认猜想③正确,请你帮助他设计实验进行验证.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液C于试管中取少量滤液C于试管中,加入足量CaCl2溶液,过滤,在滤液中滴加无色酚酞试液 | 有白色沉淀生成,溶液由无色变成红色 | 猜想③正确 |
③样品中含NaOH、CaO中的一种或两种.
19.下列实验基本操作或仪器的使用中没有错误的是( )
| A. | 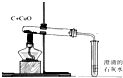 木炭还原氧化铜 | B. |  过滤 | C. |  蒸发 | D. | 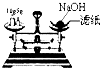 称取氯化钠固体 |
9.只用水不能区分下列各组固体物质的是( )
| A. | 生石灰、氯化钠 | B. | 碳酸钙、氢氧化钠 | C. | 蔗糖、硫酸铜 | D. | 苏打、小苏打 |
16.下表列出的是生活和工业中常用的三种漂白剂.
(1)上述漂白剂中,Ca(ClO)2属于②(填序号).①混合物 ②化合物 ③氧化物
(2)ClO2中氯元素的化合价为+4.
(3)次氯酸钙〔Ca(ClO)2〕是漂白粉的有效成分.
①次氯酸钙在潮湿的空气中久置会生成具有漂白性的物质次氯酸(HClO)和难溶于水的白色固体,反应的化学方程式Ca(ClO)2+H2O+CO2═CaCO3↓+2HClO.
②工业使用漂白粉时常根据(3)中①的反应原理,通过添加少量的B (填序号)物质来解决漂白粉漂白缓慢的问题
A.氢氧化钠 B.稀盐酸 C.氢氧化钙 D.氯化钠.
| 种类 | 亚氯 酸钠 | 二氧 化氯 | 漂白粉 |
| 化学 式 | NaClO2 | ClO2 | Ca(ClO)2和 CaCl2 |
(2)ClO2中氯元素的化合价为+4.
(3)次氯酸钙〔Ca(ClO)2〕是漂白粉的有效成分.
①次氯酸钙在潮湿的空气中久置会生成具有漂白性的物质次氯酸(HClO)和难溶于水的白色固体,反应的化学方程式Ca(ClO)2+H2O+CO2═CaCO3↓+2HClO.
②工业使用漂白粉时常根据(3)中①的反应原理,通过添加少量的B (填序号)物质来解决漂白粉漂白缓慢的问题
A.氢氧化钠 B.稀盐酸 C.氢氧化钙 D.氯化钠.
 农业技术的发展使越来越多的新鲜蔬菜水果走进人们的生活.请回答:
农业技术的发展使越来越多的新鲜蔬菜水果走进人们的生活.请回答: