题目内容
氯酸钾受热分解后,剩余固体的质量比原反应物的质量小,因此这个反应不遵守质量守恒定律.你认可这种说法吗?为什么?
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:从质量守恒定律的定义来解答.参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和,质量守恒定律适合所有的化学反应,有些反应表面上不符合质量守恒,那是忽略了某些气体反应物或生成物的质量.
解答:解:氯酸钾受热分解后的产物是氯化钾和氧气,属于化学变化,遵守质量守恒定律;
由质量守恒定律可知氯酸钾的质量等于氯化钾和氧气的质量之和,反应中由于氧气溢出,所以剩余的质量比原反应物的质量小;
答:不认可;因为氯酸钾受热分解后的产物是氯化钾和氧气,所以由质量守恒定律可知氯酸钾的质量等于氯化钾和氧气的质量之和,反应中由于氧气溢出,所以剩余的质量比原反应物的质量小.
由质量守恒定律可知氯酸钾的质量等于氯化钾和氧气的质量之和,反应中由于氧气溢出,所以剩余的质量比原反应物的质量小;
答:不认可;因为氯酸钾受热分解后的产物是氯化钾和氧气,所以由质量守恒定律可知氯酸钾的质量等于氯化钾和氧气的质量之和,反应中由于氧气溢出,所以剩余的质量比原反应物的质量小.
点评:本题主要考查学生运用质量守恒定律解答实际问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在密闭容器中,盛放A、B、C三种物质各30克,经电火花引燃,充分反应后,各物质的质量变化如下.
关于此反应,下列认识不正确的是( )
| 物质 | A | B | C | 新物质D |
| 反应前质量(克) | 30 | 30 | 30 | 0 |
| 反应后质量(克) | 待测 | 33 | 0 | 22 |
| A、该反应是分解反应 |
| B、A物质可能是单质 |
| C、变化后待测的A质量为5g |
| D、C物质中所含有的元素种类是A、B、D三种物质中所有元素种类之和 |
下列化学实验基本操作中,正确的是( )
| A、为了节约起见,将用剩下的药品放回原试剂瓶 |
| B、加热液体时,试管口朝着无人的方向 |
| C、用手直接拿固体药品 |
| D、用滴管滴加液体,滴管下端紧贴试管内壁 |
氧气是一种化学性质比较活泼的气体,它可以和许多物质发生化学反应.关于如图所示三个反应的叙述中错误的是( )


| A、都是氧化反应 |
| B、生成物都是固体 |
| C、都需要点燃 |
| D、反应都放出热量 |
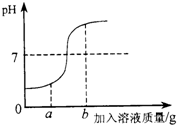 在用稀盐酸和氢氧化钙溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示.
在用稀盐酸和氢氧化钙溶液进行中和反应实验时,反应过程中溶液的酸碱度变化如图所示.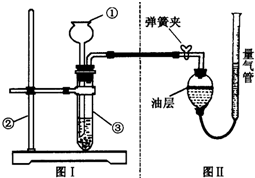 测定某石灰石样品中碳酸钙的质量分数,其方法是:将样品与稀盐酸反应,测定反应后生成CO2的体积,再根据体积换算为质量,最后根据CO2的质量求出样品中碳酸钙的质量.如图(Ⅰ)为大理石与稀盐酸反应的反应装置,图(Ⅱ)用于测量CO2的体积.
测定某石灰石样品中碳酸钙的质量分数,其方法是:将样品与稀盐酸反应,测定反应后生成CO2的体积,再根据体积换算为质量,最后根据CO2的质量求出样品中碳酸钙的质量.如图(Ⅰ)为大理石与稀盐酸反应的反应装置,图(Ⅱ)用于测量CO2的体积.