题目内容
18. 2017年“世界水日”的宣传主题是“Wastewater”(废水),如何将废水转化为有用之水是各国研究的重大课题.
2017年“世界水日”的宣传主题是“Wastewater”(废水),如何将废水转化为有用之水是各国研究的重大课题.(1)高铁酸钠(Na2FeO4)是一种处理废水的“绿色”环保高效净水剂,可由如下反应制得:Fe2O3+3X+4KOH$\frac{\underline{\;细菌\;}}{\;}$2K2FeO4+3KNO2+2H2O,则X的化学式为KNO3.
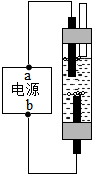
(2)如图是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氢气和氯气(Cl2),试写出该反应的化学方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;从能量变化角度看,该反应将电能转化为化学能.
分析 (1)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物X的化学式.
(2)根据反应物、生成物、反应的条件书写方程式并配平;根据能量的转化形式分析.
解答 解:(1)根据反应的化学方程式Fe2O3+3X+4KOH=2K2FeO4+3KNO2+2H2O,反应物中铁、氧、钾、氢原子个数分别为2、7、4、4,反应后的生成物中铁、氧、钾、氮、氢原子个数分别为2、16、7、3、4,根据反应前后原子种类、数目不变,则3X中含有3个钾原子、3个氮原子和9个氧原子,则每个X分子由1个钾原子、1个氮原子和3个氧原子构成,则物质X的化学式为KNO3.
(2)根据氯化钠和水在通电条件下生成氢氧化钠、氢气和氯气可知该反应的方程式为:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ 2NaOH+H2↑+Cl2↑,该反应是将电能转化为化学能;
答案:(1)KNO3;(2)2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ 2NaOH+H2↑+Cl2↑;电.
点评 本题考查的是化学反应中的能量变化以及质量守恒定律的应用,完成此题,可以依据已有的知识进行.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
8.如图是某元素的一种粒子的结构示意图,关于该粒子的说法错误的是( )


| A. | 该粒子最外层电子数为 8 | B. | 该元素为稀有气体元素 | ||
| C. | 该粒子可表示为 X3+ | D. | 该元素的核电荷数为 13 |
9.下列物质必须密封保存的是( )
| A. | 氯化钠 | B. | 浓盐酸 | C. | 石灰石 | D. | 木炭 |
13.要使如图装置中的小球扁下来,使用的固体和液体可以是( )


| A. | 小苏打和稀盐酸 | B. | 硝酸铵和水 | C. | 生石灰和水 | D. | 镁和稀硫酸 |
8.下列化学方程式与实际相符,且书写正确的是( )
| A. | 铁丝在氧气中燃烧:4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | |
| B. | 洗去试管壁上附着的铜:Cu+H2SO4=CuSO4+H2↑ | |
| C. | 用氢氧化钠溶液吸收二氧化硫:2NaOH+SO2=Na2SO4+H2O | |
| D. | 用氢氧化镁中和过多胃酸:Mg(OH)2+2HCl=MgCl2+2H2O |
