题目内容
58.8g稀盐酸恰好与100g21.2%的碳酸钠溶液完全反应.求:
(1)原稀盐酸中溶质的质量分数?
(2)反应后溶液中溶质的质量分数?
(1)原稀盐酸中溶质的质量分数?
(2)反应后溶液中溶质的质量分数?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:根据题意,由参加反应的碳酸钠溶液的质量、溶质的质量分数,由反应的化学方程式列式计算出稀盐酸中溶质的质量、生成氯化钠的质量,进而计算出溶质的质量分数即可.
解答:解:100g21.2%的碳酸钠溶液中含碳酸钠的质量为100g×21.2%=21.2g.
设原稀盐酸中溶质的质量为x,生成氯化钠的质量为y,生成二氧化碳气体的质量为z,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
21.2g x y z
=
x=14.6g
=
y=23.4g
=
z=8.8g
(1)原稀盐酸中溶质的质量分数为
×100%≈24.8%.
(2)反应后溶液中溶质的质量分数为
×100%=15.6%.
答:(1)原稀盐酸中溶质的质量分数为24.8%;(2)反应后溶液中溶质的质量分数为15.6%.
设原稀盐酸中溶质的质量为x,生成氯化钠的质量为y,生成二氧化碳气体的质量为z,
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
21.2g x y z
| 106 |
| 73 |
| 21.2g |
| x |
| 106 |
| 117 |
| 21.2g |
| y |
| 117 |
| 44 |
| 21.2g |
| z |
(1)原稀盐酸中溶质的质量分数为
| 14.6g |
| 58.8g |
(2)反应后溶液中溶质的质量分数为
| 23.4g |
| 58.8g+100g-8.8g |
答:(1)原稀盐酸中溶质的质量分数为24.8%;(2)反应后溶液中溶质的质量分数为15.6%.
点评:本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
日常生活中有很多问题都涉及化学知识,下列说法正确的是( )
| A、将废弃塑料切成碎片,混在垃圾中填埋于土壤中以减少对环境的污染 |
| B、青少年长期饮用纯净水有益于身体健康 |
| C、为了降低生产成本,可用工业酒精勾兑饮用酒 |
| D、为了使灯泡经久耐用,可在灯泡中填充氮气 |
下图是三种微粒的结构示意图,有关它们的说法正确的是( )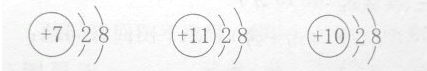
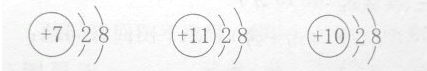
| A、它们的最外层电子数相同 |
| B、它们的核外都有两个电子层 |
| C、它们属于同种元素的微粒 |
| D、它们都是原子 |
下列实验操作中,错误的是( )
A、 |
B、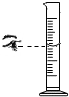 |
C、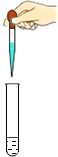 |
D、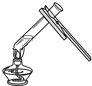 |
在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表:
则正确的说法是( )
| 物质 | A | B | C | D |
| 反应前质量/g | 4 | 6 | 111 | 4 |
| 反应后质量/g | 待测 | 15 | 0 | 84 |
| A、该反应的反应物为A和C |
| B、容器中发生的化学反应,属于化合反应 |
| C、反应后,待测A的质量为26g |
| D、化学反应中A与B质量比26:9 |
含有游离态氧元素的物质是( )
| A、H2 |
| B、O2 |
| C、H2O |
| D、H2O2 |
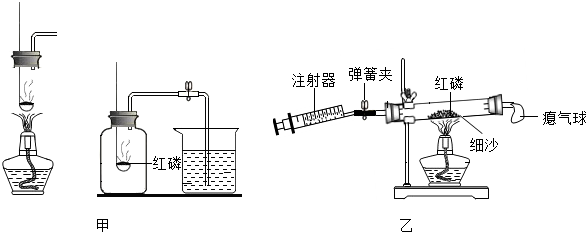
 完成下列实验,你会从中感受到许多乐趣.
完成下列实验,你会从中感受到许多乐趣.