题目内容
某小组对测定空气中氧气体积分数的实验进行了如下研究
①选用汞、磷、铜等物质均可以完成该实验,选择反应物的依据是 .
A、反应物是固体 B、在空气中反应且只消耗氧气
C、燃烧有明显现象 D、生成物不是气体
②用甲、乙两套装置进行实验(红磷充足、装置不漏气).红磷燃烧的化学方程式是 ,有关分析合理的是 .
A、都只能在实验结束后,推得氮气是无色气体
B、甲中燃烧匙伸入集气瓶太慢,测得空气中氧气的体积分数将偏大
C、乙中的瘪气球可以防止燃烧放热使橡胶塞弹出
D、乙比甲更节约能源
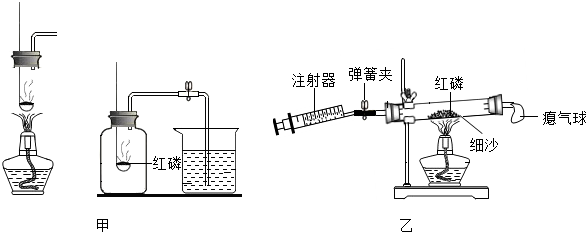
③利用乙装置实验时,先关闭弹簧夹,加热使红磷反应,待装置冷却至室温后打开弹簧夹.反应前后各数据及结论如下.
①选用汞、磷、铜等物质均可以完成该实验,选择反应物的依据是
A、反应物是固体 B、在空气中反应且只消耗氧气
C、燃烧有明显现象 D、生成物不是气体
②用甲、乙两套装置进行实验(红磷充足、装置不漏气).红磷燃烧的化学方程式是
A、都只能在实验结束后,推得氮气是无色气体
B、甲中燃烧匙伸入集气瓶太慢,测得空气中氧气的体积分数将偏大
C、乙中的瘪气球可以防止燃烧放热使橡胶塞弹出
D、乙比甲更节约能源

③利用乙装置实验时,先关闭弹簧夹,加热使红磷反应,待装置冷却至室温后打开弹簧夹.反应前后各数据及结论如下.
| 玻璃管中原有 空气的体积 | 注射器中气体的体积 | 结论 | |
| 反应前 | 反应后 | ||
| 40 mL | 30 mL | 氧气约占空气体积的五分之一 | |
考点:测定空气里氧气含量的探究,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:①测定空气中氧气体积分数的实验中最适合物质应该具备的条件是:一定条件下能在空气中氧气反应,生成物不能是气体.
②红磷燃烧生成五氧化二磷;根据红磷测定空气里氧气含量的实验原理、操作步骤、注意事项进行分析.
③根据氧气约占空气体积的五分之一推算.
②红磷燃烧生成五氧化二磷;根据红磷测定空气里氧气含量的实验原理、操作步骤、注意事项进行分析.
③根据氧气约占空气体积的五分之一推算.
解答:解:①测定空气中氧气体积分数的实验中最适合物质应该具备的条件是:一定条件下能在空气中氧气反应,生成物不能是气体.
②红磷燃烧的化学方程式为:4P+5O2
2P2O5;
A、甲、乙两套装置进行实验都可以得到氧气约占空气体积的五分之一等,故错误;
B、甲中燃烧匙伸入集气瓶太慢,燃烧生成的热使气体膨胀,使装置中的气体减少,测得空气中氧气的体积分数将偏大,正确;
C、乙中红磷燃烧时放出大量的热,使装置中气体膨胀,瘪气球可以防止燃烧放热使橡胶塞弹出,正确;
D、乙比甲都需要加热使红磷燃烧,无法区分哪个更节约能源,故错误.
③由于氧气约占空气体积的五分之一,所以假设玻璃管中原有空气的体积为X,
则X×
=(40mL-30mL)
所以X=50mL
故答案为:①BD;②4P+5O2
2P2O5;BC;③50.
②红磷燃烧的化学方程式为:4P+5O2
| ||
A、甲、乙两套装置进行实验都可以得到氧气约占空气体积的五分之一等,故错误;
B、甲中燃烧匙伸入集气瓶太慢,燃烧生成的热使气体膨胀,使装置中的气体减少,测得空气中氧气的体积分数将偏大,正确;
C、乙中红磷燃烧时放出大量的热,使装置中气体膨胀,瘪气球可以防止燃烧放热使橡胶塞弹出,正确;
D、乙比甲都需要加热使红磷燃烧,无法区分哪个更节约能源,故错误.
③由于氧气约占空气体积的五分之一,所以假设玻璃管中原有空气的体积为X,
则X×
| 1 |
| 5 |
所以X=50mL
故答案为:①BD;②4P+5O2
| ||
点评:本题考查了实验室探究空气中氧气的含量,对实验成功的操作进行了系统性的考查,有利于培养学生的实验操作能力和严谨科学的实验态度,特别是对分析实验能力的培养.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
化学用语是学习、交流化学的通用语言,下列化学用语表示意义最多的是( )
| A、N2 |
| B、2H2O |
| C、4P |
| D、Fe3+ |
现有一常见的物质M,其燃烧反应的化学方程式:M+3O2
2CO2+3H2O,试推测M的化学式为( )
| ||
| A、CH4 |
| B、C2H6 |
| C、CH30H |
| D、C2H50H |
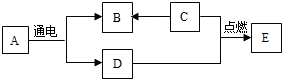 A、B、C、D、E五中物质之间的变化关系如图所示,其中B、C、D是单质,C为钢铁的主要成分.试回答:
A、B、C、D、E五中物质之间的变化关系如图所示,其中B、C、D是单质,C为钢铁的主要成分.试回答: