题目内容
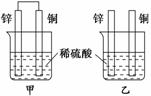 将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,下列叙述正确的是
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,下列叙述正确的是
( )。
A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大
D.产生气泡的速率甲比乙慢
解析 甲烧杯中铜片表面有H2产生(原电池),乙烧杯中锌片表面有气泡产生;甲中铜片是正极,乙不是原电池(置换反应);两烧杯中溶液的pH均增大;原电池的原因使产生气泡的速率甲比乙快。
答案 C

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10克样品放入烧杯中,再取60克稀硫酸分六次加入烧杯中,充分反应,实验数据如下:
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | 第六次 | |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.35 | 8.7 | 8.05 | 7.4 | 6.75 | 6.75 |
(1)黄铜样品中锌的质量分数为多少?(写出计算步骤,下同)
(2)反应过程中产生氢气的质量是多少?
(3)最后烧杯中所盛物质的总质量是多少?
碳单质在工业上有多种用途。例如焦炭可用来制取水煤气、冶炼金属,活性炭可处理大气污染物NO。
一定条件下,在2 L密闭容器中加入NO和活性炭(无杂质)反应生成气体A和B。当温度在T1 ℃时,测得各物质平衡时物质的量如下表:
| 活性炭 | NO(mol) | A(mol) | B(mol) | |
| 初始 | 2.030 | 0.100 | 0 | 0 |
| 平衡 | 2.000 | 0.040 | 0.030 | 0.030 |
(1)该反应方程式为_______________________________________________________。
(2)在T1 ℃下反应达到平衡后,下列措施能改变NO的转化率的是________(填字母序号)。
a.增大活性炭的量 b.增大压强
c.升高温度 d.移去部分B
(3)结合上表数据,该反应的平衡常数表达式为____________________________________(生成物A、B用相应的化学式表示)。若T1 ℃时的平衡常数为K1,T2 ℃时的平衡常数为K2,且K1>K2,能否判断该反应是吸热反应还是放热反应,说明理由_____________________。
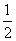 O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1