题目内容
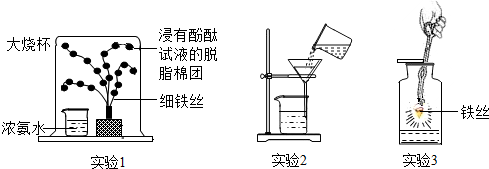
6.下列实验操作或方法正确的是( )| A. | 将空气通过灼热的铜网可以除去氧气; 用食盐水制作叶脉书签 | |
| B. | 用点燃的方法可以除去二氧化碳中的一氧化碳; 用石蕊溶液鉴别稀盐酸和稀硫酸 | |
| C. | 将冷碟子放在蜡烛火焰的上方,得到炭黑; 用加碱溶液的方法区别氯化铵与氯化钠 | |
| D. | 电解水得到的H2和O2质量比为2:1; 用食盐水除水垢 |
分析 A、根据氧气能够与铜反应分析;叶脉书签就是除去表皮和叶肉组织,而只由叶脉做成;植物的叶、叶脉由坚韧的纤维素构成,在碱液中不易煮烂,而叶脉四周的叶肉在碱液中容易煮烂;
B、根据少量的一氧化碳在二氧化碳中不会燃烧分析;根据稀盐酸和稀硫酸均显酸性,进行分析判断;
C、根根据蜡烛不完全燃烧产生炭黑分析;氯化铵是铵态氮肥,能与碱混合产生有刺激性气味的氨气;
D、氢气和氧气的体积比为2:1,食盐和水垢不能反应.
解答 解:A、叶脉书签就是除去表皮和叶肉组织,而只由叶脉做成;植物的叶、叶脉由坚韧的纤维素构成,在碱液中不易煮烂,而叶脉四周的叶肉在碱液中容易煮烂,食盐不具有碱性,故不能制作叶脉书签,故错误;
B、少量的一氧化碳在不支持燃烧的二氧化碳中不会燃烧;稀盐酸和稀硫酸均显酸性,均能使石蕊溶液变红色,无法鉴别,故错误;
C、将冷碟子放在蜡烛火焰的上方,蜡烛会发生不完全燃烧产生炭黑,氯化铵是铵态氮肥,能与碱混合产生有刺激性气味的氨气,而氯化钠与碱混合没有现象,可以鉴别,故正确;
D、电解水得到的H2和O2体积比为2:1;水垢的主要成分是碳酸钙和氢氧化镁,它们都不和氯化钠反应,故错误.
故选C.
点评 利用所要鉴别物质的性质差别,设计实验,实验中出现明显的现象差异,达到鉴别物质的目的.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.做化学实验应当特别注意安全.以下几种实验操作不正确的是( )
| A. |  取用粉末状药品 | B. |  点燃酒精灯 | ||
| C. |  向试管中倾倒液体 | D. |  称取氢氧化钠固体 |
9.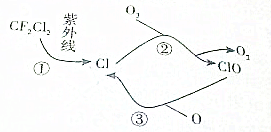 卤代烷烃曾用作冰箱制冷剂,但在高空中与某些气体发生反应,破坏臭氧层,而被逐渐淘汰.如氟氯甲烷(CF2Cl2)在高空中会发生如图所示的变化,根据图示,判断下列说法中不正确的是( )
卤代烷烃曾用作冰箱制冷剂,但在高空中与某些气体发生反应,破坏臭氧层,而被逐渐淘汰.如氟氯甲烷(CF2Cl2)在高空中会发生如图所示的变化,根据图示,判断下列说法中不正确的是( )
 卤代烷烃曾用作冰箱制冷剂,但在高空中与某些气体发生反应,破坏臭氧层,而被逐渐淘汰.如氟氯甲烷(CF2Cl2)在高空中会发生如图所示的变化,根据图示,判断下列说法中不正确的是( )
卤代烷烃曾用作冰箱制冷剂,但在高空中与某些气体发生反应,破坏臭氧层,而被逐渐淘汰.如氟氯甲烷(CF2Cl2)在高空中会发生如图所示的变化,根据图示,判断下列说法中不正确的是( )| A. | ②过程发生的变化是:Cl+O2→ClO+O2 | B. | ③过程发生的变化是:ClO+O→Cl+O2 | ||
| C. | Cl反复作用使O3不断转变为O2 | D. | 氟氯甲烷是上述总反应的催化剂 |
14.下列各组物质能在水溶液中大量共存的是( )
| A. | HCl、NaOH、H2SO4 | B. | AgNO3、HNO3、BaCl2 | ||
| C. | Fe2(SO4)3、NaCl、KOH | D. | FeCl3、Na2SO4、KNO3 |
1.现含有HCl和氯化铜的混合溶液50g,将160g溶质的质量分数为10%的氢氧化钠溶液平均分四次加入到该混合液中,生成沉淀的质量与加入氢氧化钠的溶液的质量关系如表.
(1)第四次加入氢氧化钠,溶液中的溶质有NaCl、NaOH;(填化学式)
(2)求混合溶液中氯化铜的质量分数.(写出计算过程)
(3)画出在该混合溶液中加入氢氧化钠溶液质量与生成沉淀质量变化关系的曲线(请在答题卷上面,并标出折点坐标)
| 次数 | 1 | 2 | 3 | 4 |
| 加入氢氧化钠溶液的质量合计/g | 40 | 80 | 120 | 160 |
| 生成的沉淀质量/g | 0 | 4.9 | 9.8 | 9.8 |
(2)求混合溶液中氯化铜的质量分数.(写出计算过程)
(3)画出在该混合溶液中加入氢氧化钠溶液质量与生成沉淀质量变化关系的曲线(请在答题卷上面,并标出折点坐标)
11.根据所给信息写出相关的化学方程式:
(1)稀盐酸可破坏铝锅表面的氧化膜(主要成分是Al2O3);
(2)胃酸过多时,可服用氢氧化镁药品来减轻症状;
(3)丁烷(C4H10)完全燃烧生成CO2和H2O.
(1)稀盐酸可破坏铝锅表面的氧化膜(主要成分是Al2O3);
(2)胃酸过多时,可服用氢氧化镁药品来减轻症状;
(3)丁烷(C4H10)完全燃烧生成CO2和H2O.
15.如图实验装置进行的相应实验,达不到实验目的是( )
| A. |  用如图所示装置除去CO2中含有的少量HCl气体 | |
| B. | 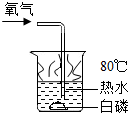 用如图所示的装置证明可燃物燃烧需要与氧气接触 | |
| C. | 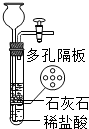 用如图所示装置制取少量CO2气体 | |
| D. |  在实验室中,用如图所示装置除去少量黄河水中的泥沙 |
 化学与生活、生产关系密切.请回答下列问题:
化学与生活、生产关系密切.请回答下列问题: