题目内容
1.现含有HCl和氯化铜的混合溶液50g,将160g溶质的质量分数为10%的氢氧化钠溶液平均分四次加入到该混合液中,生成沉淀的质量与加入氢氧化钠的溶液的质量关系如表.| 次数 | 1 | 2 | 3 | 4 |
| 加入氢氧化钠溶液的质量合计/g | 40 | 80 | 120 | 160 |
| 生成的沉淀质量/g | 0 | 4.9 | 9.8 | 9.8 |
(2)求混合溶液中氯化铜的质量分数.(写出计算过程)
(3)画出在该混合溶液中加入氢氧化钠溶液质量与生成沉淀质量变化关系的曲线(请在答题卷上面,并标出折点坐标)
分析 稀盐酸和氢氧化钠反应生成氯化钠和水,氯化铜和氢氧化钠反应生成氢氧化铜沉淀和氯化钠,根据提供的数据和反应的化学方程式可以进行相关方面的计算和判断.
解答 解:(1)第四次加入氢氧化钠,氢氧化钠过量,溶液中的溶质有NaCl、NaOH.
故填:NaCl、NaOH.
(2)设氯化铜质量为x,
2NaOH+CuCl2=Cu(OH)2↓+2NaCl,
135 98
x 9.8g
$\frac{135}{x}$=$\frac{98}{9.8g}$,
x=13.5g,
混合溶液中氯化铜的质量分数为:$\frac{13.5g}{50g}$×100%=27%,
答:混合溶液中氯化铜的质量分数为27%.
(3)在该混合溶液中加入氢氧化钠溶液质量与生成沉淀质量变化关系的曲线如下图所示: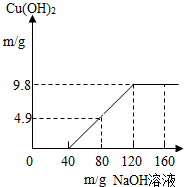
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.如图为汽车尾气净化装置中发生反应的微观示意图,有关叙述错误的是( )


| A. | 该装置可净化汽车尾气 | B. | 图中单质的化学式为N2 | ||
| C. | 反应后分子总数减少 | D. | 该反应是置换反应 |
4.下列图象与事实相符的是( )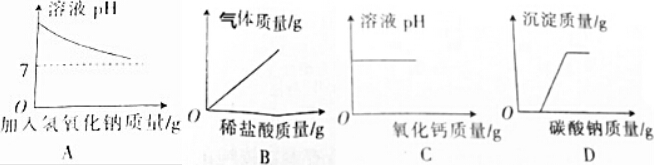

| A. | 向一定量的盐酸中加入氢氧化钠 | |
| B. | 向一定质量的石灰石中加入过量的稀盐酸 | |
| C. | 向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体 | |
| D. | 向含有盐酸和CaCl2的混合溶液中加入Na2CO3溶液 |
9.浓盐酸若敞口放置在瓶口会看到( )
| A. | 白烟 | B. | 白雾 | C. | 白色烟雾 | D. | 盐酸小液滴 |
6.下列实验操作或方法正确的是( )
| A. | 将空气通过灼热的铜网可以除去氧气; 用食盐水制作叶脉书签 | |
| B. | 用点燃的方法可以除去二氧化碳中的一氧化碳; 用石蕊溶液鉴别稀盐酸和稀硫酸 | |
| C. | 将冷碟子放在蜡烛火焰的上方,得到炭黑; 用加碱溶液的方法区别氯化铵与氯化钠 | |
| D. | 电解水得到的H2和O2质量比为2:1; 用食盐水除水垢 |
10.下列各组离子在无色溶液中能大量共存的是( )
| A. | Ag+、K+、NO3-、Cl- | B. | Na+、Ba2+、NO3-、OH- | ||
| C. | Cu2+、Mg2+、Cl-、NO3- | D. | H+、Ca2+、CO32-、OH- |
 据报道,全球每年浪费掉的粮食约有1000亿吨,其中,约300亿吨是加工过后食品.如图所示是一包烤花生的图片,图中的脱氧剂在食品防腐保鲜,特别是对延长含高油脂食品的保质期有着重要作用.请回答下列问题:
据报道,全球每年浪费掉的粮食约有1000亿吨,其中,约300亿吨是加工过后食品.如图所示是一包烤花生的图片,图中的脱氧剂在食品防腐保鲜,特别是对延长含高油脂食品的保质期有着重要作用.请回答下列问题: