题目内容
5.物质发生化学变化的前后,总质量是否发生改变?是增加、减小还是不变呢?甲、乙、丙三位同学按下面的步骤进行探究:(1)提出假设:物质发生化学变化前后总质量不变.
(2)设计并进行实验,甲设计的实验装置和选用的药品如图A所示,乙设计的实验装置和选用药品如图B所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察.
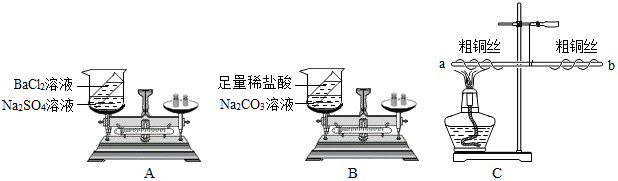
写出A、B两个实验发生反应的化学方程式:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,Na2CO3+2HCl=2NaCl+H2O+CO2↑.丙进行了图C所示的实验,在一根用细铜丝吊着的长玻璃棒两端,分别绕上粗铜丝,并使玻璃棒保持水平.然后,用酒精灯给a端铜丝加热数分钟.停止加热后冷却,他观察到的现象是a端上铜丝变黑、玻璃棒a端下沉.
(3)实验结论:
甲认为:在化学反应中,生成物的总质量与反应物的总质量相等;
乙、丙认为:在化学反应中,生成物的总质量与反应物的总质量不相等.
(4)你认为甲的结论正确,请从原子的角度分析,结论正确的理由是:在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.
(5)导致其他实验结论错误的原因是B实验反应后生成的气体逸散到空气中去了,C实验a端铜丝增加了氧元素的质量.因此,如果有气体参与反应或者生成物中有气体的反应,则一定要设计反应在密闭装置中进行.
分析 (2)根据反应物和复分解反应的原理书写化学方程式.铜在加热的条件下会与氧气反应生成氧化铜,会使铜丝质量增加.
(4)化学反应的过程实际上是原子的重新组合过程,原子的数目、质量、种类不会增减.
(5)在验证质量守恒定律时,若有气体参加或生成的实验必须在密闭的环境中进行.
解答 解:(2)由图示可知发生的反应是红磷燃烧,故答案为:
4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5
根据反应物是碳酸钠和盐酸及复分解反应的原理可知,生成物是氯化钠、水和二氧化碳,故答案为:
Na2CO3+2HCl=2NaCl+H2O+CO2↑;
铜在加热的条件下会与氧气反应生成黑色的氧化铜,会使铜丝质量增加,会使左端下沉,故答案为:
a端上铜丝变黑;玻璃棒a端下沉;
(4)化学反应的过程实际上是原子的重新组合过程,原子的数目、质量、种类不会增减,故答案为:
甲;在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变;
(5)在验证质量守恒定律时,若有气体参加或生成的实验必须在密闭的环境中进行,生成物的质量等于参加的反应物的质量之和,故答案为:
B实验反应后生成的气体逸散到空气中去了;
C实验a端铜丝增加了氧元素的质量;
有气体参与反应或者生成物中有气体.
答案:
(1)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(2)a端上铜丝变黑;玻璃棒a端下沉;
(4)甲;在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变;
(5)B实验反应后生成的气体逸散到空气中去了;C实验a端铜丝增加了氧元素的质量;有气体参与反应或者生成物中有气体.
点评 在验证质量守恒定律时,有气体参加的实验必须密封,若不密封所得的生成物的质量与反应物的质量不相等,不能得出质量守恒的结论.

 阅读快车系列答案
阅读快车系列答案| A. | 试管 | B. | 集气瓶 | C. | 烧杯 | D. | 量筒 |
| A. | 全面关停化工企业 | B. | 限制生产含磷洗涤剂 | ||
| C. | 改进汽车尾气净化技术 | D. | 对煤进行脱硫处理 |

 铜梁巴川中学化学兴趣小组为测定某矿山开采的石灰石样品中碳酸钙的质量.进行下列操作:取6g石灰石样品,将其敲碎后,放入烧杯内(烧杯质量为20g).再加入50g足量的稀盐酸使其完全反应(杂质不与盐酸反应).反应所需时间(t)和烧杯及其所盛物质总重量(m)的关系如图所示.试回答:
铜梁巴川中学化学兴趣小组为测定某矿山开采的石灰石样品中碳酸钙的质量.进行下列操作:取6g石灰石样品,将其敲碎后,放入烧杯内(烧杯质量为20g).再加入50g足量的稀盐酸使其完全反应(杂质不与盐酸反应).反应所需时间(t)和烧杯及其所盛物质总重量(m)的关系如图所示.试回答:


 如图是测定空气中氧气组成的装置.请回答下列问题:
如图是测定空气中氧气组成的装置.请回答下列问题: