题目内容
13.化学和我们的生活密切相关,根据所学,回答下列问题.(1)我们平阴是全国著名的玫瑰之乡,每年5月份正是玫瑰花开香如海时节,由玫瑰花提炼的玫瑰油比黄金还要贵,芳樟醇是玫瑰油的成分之一,分子式为C10H18O,具有浓甜香味,芳樟醇分子中碳、氢元素质量之比为20:3.
(2)因为CO2含量不断升高,全球气候问题日趋严重,所以我们不仅要努力减少CO2的排放,还应努力将CO2转化为有用物质,为了实现这一想法,研究人员设计了利用NaOH溶液来“捕捉”CO2,并将CO2收集利用的流程,如图(部分条件及物质未标出).
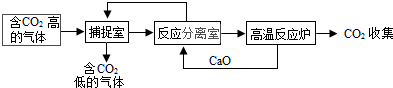
下列有关该流程的叙述正确的是D
A.该流程可实现CO2零排放
B.该流程优点是能耗小
C.整个流程中,可以循环利用的物质有一种
D.二氧化碳“捕捉”室中氢氧化钠溶液喷成雾状有利于吸收二氧化碳
(3)我国科学家发现用含硒(Se)化合物亚硒酸钠能消除掉加速人体衰老的活性氧,亚硒酸钠中的硒元素为+4价,则亚硒酸钠的化学式为C
A.NaSeO3 B.Na2SeO4 C.Na2SeO3 D.Na2SeO2
(4)我们国家高铁迅速发展,因为它的快捷性,已经成为我们出行的热选交通工具,高铁建设需要消耗大量的铝、铁等金属,工业上常用电解氧化铝的方法冶炼金属铝,该反应属于B(填字母序号).
A.化合反应 B.分解反应 C.置换反应 D.复分解反应.
分析 (1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比;进行解答;
(2)根据流程图中的信息,进行分析;
(3)根据化学式中各元素的化合价代数和为零的原则,把三种元素的化合价代入公式中,根据是否等于0判断正确选项.
(4)根据反应物与生成物进行分析解答.
解答 解:(1)芳樟醇分子中碳、氢元素质量之比为:(12×10):18=20:3;故填:20:3;
(2)根据题干提供的信息进行分析,碳酸钙高温能分解生成氧化钙和二氧化碳;增大反应物的接触面积能促进反应的进行;氧化钙能与水反应生成氢氧化钙,氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠;而氢氧化钠溶液可来“捕捉”CO2;故该过程只有碳酸钙、氢氧化钠等都可以循环利用;而含有二氧化碳含量低的气体排出,并没有“实现CO2零排放”;碳酸钙高温能分解生成氧化钙和二氧化碳,需要消耗能源;二氧化碳“捕捉”室中氢氧化钠溶液喷成雾状有利于吸收二氧化碳;
(3)A.+1+(+4)+(-2)×3=-1,故错;
B.(+1)×2+(+4)+(-2)×4=-2,故错;
C.(+1)×2+(+4)+(-2)×3=0,故对;
D.(+1)×2+(+4)+(-2)×2=+2,故错.
(4)电解氧化铝生成铝和氧气,该反应符合“一变多”的特征,属于分解反应.
故答案为:(1)20:3;(2)D;(3)C;(4)B.
点评 本题考查学生的识图能力,识图时一定要仔细,要分析到方方面面,不要漏掉重要的信息.本题考查了吸收二氧化碳的方法,完成此题,可以依据已有的知识结合二氧化碳的性质进行,书写反应的化学方程式要注意配平.

练习册系列答案
相关题目
4.下列实验操作正确的是( )
| A. | 固体反应物在试管中加热时,试管口向上倾斜,以免固体漏出 | |
| B. | 用托盘天平称量物质时,直接用手取出砝码 | |
| C. | 实验室化学反应后的废液都直接倒入下水道 | |
| D. | 玻璃仪器洗涤干净的标准是内壁附着的水既不聚成水滴也不成股流下 |
18. 实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.
实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.
【提出问题】这瓶无色溶液究竟是什么物质的溶液?
【猜想与假设】经了解得知,这瓶无色溶液原是放在存放盐溶液的柜子里.由此猜测:可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
【理论分析】为了确定该溶液,他们首先进行了分析:
(1)甲同学根据标签上的组成元素认为一定不可能是氯化钠溶液.乙同学依据碳酸氢钠和硝酸钠的化学式中钠的原子个数为1,而标签中为2,提出,该溶液也不可能是碳酸氢钠、硝酸钠的溶液.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
【实验结论】
(2)该瓶无色溶液的溶质是碳酸钠.生成白色沉淀的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
【实验反思】
(3)丙同学认为原设计的实验还可简化,同样达到鉴别的目的.丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
 实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.
实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.【提出问题】这瓶无色溶液究竟是什么物质的溶液?
【猜想与假设】经了解得知,这瓶无色溶液原是放在存放盐溶液的柜子里.由此猜测:可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
【理论分析】为了确定该溶液,他们首先进行了分析:
(1)甲同学根据标签上的组成元素认为一定不可能是氯化钠溶液.乙同学依据碳酸氢钠和硝酸钠的化学式中钠的原子个数为1,而标签中为2,提出,该溶液也不可能是碳酸氢钠、硝酸钠的溶液.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
| 实验操作 | 实验现象 |
| ①取少量该无色溶液于试管中,慢慢滴加BaC12溶液 ②静置后,倾去上层清液,向沉淀中滴加稀盐酸 | 产生白色沉淀 产生大量气泡,沉淀消失. |
(2)该瓶无色溶液的溶质是碳酸钠.生成白色沉淀的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
【实验反思】
(3)丙同学认为原设计的实验还可简化,同样达到鉴别的目的.丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
| 实 验 操 作 | 实 验 现 象 |
| 取上述无色溶液少许于试管中,滴加少量的稀盐酸 | 溶液中有气泡产生 |
3.在一密闭容器内有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质质量如表,该密闭容器中发生的反应属于:( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前物质质量/g | 4 | 5 | 84 | 6 |
| 反应后物质质量/g | 待测 | 27 | 0 | 15 |
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.

 归纳总结是学习化学的重要方法,小明同学用图总结了Na2CO3的部分化学性质.
归纳总结是学习化学的重要方法,小明同学用图总结了Na2CO3的部分化学性质.