题目内容
10.如图为某化学反应的微观模拟图,其中“ ”表示氧原子,“
”表示氧原子,“ ”表示碳原子,“
”表示碳原子,“ ”表示氢原子.则下列说法不正确的是( )
”表示氢原子.则下列说法不正确的是( )
| A. | 生成物丙和丁都是氧化物 | |
| B. | 反应物甲、乙两种分子的个数比为1:3 | |
| C. | 甲物质中碳、氧元素的质量比为3:2 | |
| D. | 化学反应前后氧元素的化合价不变 |
分析 根据化学反应的微观模拟图,A的化学式为C2H6O,B的化学式为O2,C的化学式为CO2,D的化学式为H2O,反应的化学方程式为C2H6O+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O,然后根据反应特点分析判断各选项.
解答 解:根据化学反应的微观模拟图,A的化学式为C2H6O,B的化学式为O2,C的化学式为CO2,D的化学式为H2O,反应的化学方程式为C2H6O+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O,因此:
A、生成物是CO2和H2O都是由两种元素组成的纯净物,且含有氧元素,属于氧化物,故说法正确;
B、观察微观示意图结合方程式可知反应物甲、乙两种分子的个数比为1:3,故说法正确;
C、甲物质是C2H6O,其中碳、氧元素的质量比为(12×2):16=3:2,故说法正确;
D、反应前的氧元素以单质的形式存在,化合价为0,变成化合物,元素的化合价一定发生改变,故说法出错误;
故选项为:D.
点评 本题属于微观示意图的考查,根据变化微观示意图及粒子构成模拟图,书写反应的方程式,正确判断变化中的物质构成是解答本题的基本方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列各组物质在pH=14的某无色溶液中,能大量共存的是( )
| A. | FeCl3 NaCl KNO3 | B. | NaCl NaOH NaNO3 | ||
| C. | CaCl2 NaNO3 Na2CO3 | D. | KNO3 H2SO4 NaCl |
1.比较与分析归纳是学习化学的常用方法.请比较表中信息,回答有关问题:
(1)氟单质的状态气态;溴原子结构中的X=35;碘单质的化学式I2;碘元素位于第5周期;
(2)氟原子容易得到电子,形成的离子与Ca2+形成化合物的化学式为CaF2;
(3)试归纳氟、氯、溴、碘的原子结构规律(答一点即可):氟、氯、溴、碘原子的最外层电子数相同等;
(4)HBr的化学性质与HCl相似,试写出HBr与小苏打反应的化学方程式:NaHCO3+HBr=NaBr+H2O+CO2↑.
| 元素名称 | 氟 | 氯 | 溴 | 碘 |
| 元素符号 | F | Cl | Br | I |
| 原子结构 示意图 | 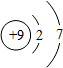 |  | 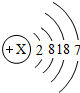 | 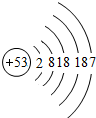 |
| 单质化学式 | F2 | Cl2 | Br2 | |
| 常温常压下 | 气态 | 液态 | 固态 |
(2)氟原子容易得到电子,形成的离子与Ca2+形成化合物的化学式为CaF2;
(3)试归纳氟、氯、溴、碘的原子结构规律(答一点即可):氟、氯、溴、碘原子的最外层电子数相同等;
(4)HBr的化学性质与HCl相似,试写出HBr与小苏打反应的化学方程式:NaHCO3+HBr=NaBr+H2O+CO2↑.
15.实验室可利用碱式碳酸铜(化学式:Cu2(OH)2CO3)制备氧化铜,并进行碳粉还原氧化铜的实验.
①制备氧化铜并检验产物,装置如图1所示(省略夹持仪器):

步骤一:连接A和B,打开活塞,通入空气.步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热.
B中发生反应的化学方程式为:Cu2(OH)2CO3═2CuO+X+CO2↑X是H2O.C中试剂是无水硫酸铜.A的作用是吸收空气中的水蒸气和二氧化碳,防止对产物检验造成干扰.选择t3时停止加热的理由是固体质量不再减少,证明碱式碳酸铜已经完全分解.
②一定量碳粉还原①中制得的氧化铜并检验产物,装置如图2所示:实验过程中,观察到F中溶液变浑浊,E中的现象是黑色粉末变成红色;反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是F中的液体通过导管流入E中,造成试管炸裂.
③分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因.不能确定炭粉还原氧化铜的生成物中是否含有二氧化碳.
因为可能有①中未分解的碱式碳酸铜在实验②中分解,产生二氧化碳气体,干扰对炭粉还原氧化铜反应生成物的判断.
①制备氧化铜并检验产物,装置如图1所示(省略夹持仪器):

步骤一:连接A和B,打开活塞,通入空气.步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热.
| 加热时间(min) | 0 | T1 | T2 | T3 |
| B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
②一定量碳粉还原①中制得的氧化铜并检验产物,装置如图2所示:实验过程中,观察到F中溶液变浑浊,E中的现象是黑色粉末变成红色;反应完全后,若仅撤走酒精喷灯停止加热,可能导致的后果是F中的液体通过导管流入E中,造成试管炸裂.
③分析:若①中省略步骤三,对②中反应产物判断可能产生的影响及其原因.不能确定炭粉还原氧化铜的生成物中是否含有二氧化碳.
因为可能有①中未分解的碱式碳酸铜在实验②中分解,产生二氧化碳气体,干扰对炭粉还原氧化铜反应生成物的判断.
19.根据质量守恒定律判断:X+2O2=CO2+2H2O中,X的化学式为( )
| A. | CH3OH | B. | CH3COOH | C. | C2H5OH | D. | CH4 |
1.向10g部分变质了的烧碱固体中,加入73g溶质质量分数为10%的稀盐酸,恰好完全反应,则反应后溶液中溶质的质量为( )
| A. | 11.7g | B. | 5.85g | C. | 10g | D. | 4g |
 如图表示向CuCl2溶液中加入过量的锌片反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号):
如图表示向CuCl2溶液中加入过量的锌片反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号): :Cu2+、
:Cu2+、 :Cl-、
:Cl-、 :Zn2+.
:Zn2+.