题目内容
用50g质量分数为14.6%的稀盐酸与足量的大理石反应,生成二氧化碳的体积(标准状况下)是多少?(在标准状况下,二氧化碳的密度为1.98g/L)(计算结果精确到0.1)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:大理石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,根据稀盐酸的质量及其质量分数可以计算生成二氧化碳的质量,根据二氧化碳的密度可以计算二氧化碳的体积.
解答:解:设生成二氧化碳的质量为x,
稀盐酸中氯化氢的质量为:50g×14.6%=7.3g,
CaCO3+2HCl═CaCl2+CO2↑+H2O,
73 44
7.3g x
=
,
x=4.4g,
生成二氧化碳的体积为:4.4g÷1.98g/L=2.2L,
答:生成二氧化碳的体积是2.2L.
稀盐酸中氯化氢的质量为:50g×14.6%=7.3g,
CaCO3+2HCl═CaCl2+CO2↑+H2O,
73 44
7.3g x
| 73 |
| 7.3g |
| 44 |
| x |
x=4.4g,
生成二氧化碳的体积为:4.4g÷1.98g/L=2.2L,
答:生成二氧化碳的体积是2.2L.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
如图所示实验操作正确的是( )
A、 |
B、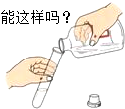 |
C、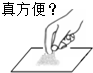 |
D、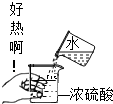 |
为了保护环境,使垃圾资源化,广州市已实行将城市废品进行分类处理下列可回收废品属于同类物质的是( )
| A、废电池、硬纸板 |
| B、易拉罐、废铜烂铁 |
| C、空啤酒瓶、塑料袋 |
| D、废旧报纸、包装塑料 |
垃圾是放错地方的资源,下列物品中可回收利用的是( )
| A、果皮 | B、烂铁锅 |
| C、破碎的啤酒瓶 | D、霉变大米 |
下列各组物质中,能反应且生成物是硫酸亚铁的是( )
| A、氧化铁+稀硫酸 |
| B、氢氧化铁+硫酸 |
| C、氢氧化铁+硫酸钡 |
| D、铁+稀硫酸 |
 ”表示一个氢原子,则“
”表示一个氢原子,则“ ”表示的微粒是
”表示的微粒是 (1)如图所示是KN03和NaCl两种物质的溶解度曲线,请回答下列问题:
(1)如图所示是KN03和NaCl两种物质的溶解度曲线,请回答下列问题: